Última parte del examen simulador de química para las carreras del área de ciencias médico biológicas del examen de admisión al IPN. Para esta última parte vamos a resolver los reactivos del 61 al 75.

¡Muy buen trabajo! Has llegado a la quinta y última versión de la serie de exámenes simulacro de química del área CMB del IPN, los cuales son una herramienta para mejorar tus habilidades a la hora de presentar la prueba real de ingreso al IPN.
Reactivo 61
Para separar un material magnético de otros que no presentan la misma propiedad ¿Qué método se utiliza?
- Filtración.
- Tamizaje.
- Decantación.
- Imantación.
Solución:
La imantación es un método basado en la separación de un material magnético de otro que no posee dicha propiedad con el uso de un imán.
La imantación aprovecha la propiedad física del magnetismo, por lo tanto, solo es útil para ciertas sustancias como:
- Ferromagnéticas: Materiales fuertemente afectados por campos magnéticos.
- Paramagnéticas: Materiales parcialmente afectados por campos magnéticos.
Respuesta correcta opción D.
Reactivo 62
Las __________________ se descomponen en sustancias más simples o elementos constituyentes.
- Sustancias simples.
- Sustancias compuestas.
- Elementos.
- Sustancias puras.
Solución:
Las sustancias compuestas, mediante determinados procesos químicos, pueden ser separadas en sustancias más simples o en sus elementos constituyentes. A diferencia de las sustancias puras o elementos, los cuales no pueden ser separados en unidades más sencillas.
Respuesta correcta opción B.
Reactivo 63
¿Cuál es el único metal que se encuentra en estado líquido en la naturaleza y es altamente tóxico para el ser humano?
- Neodimio.
- Samario.
- Mercurio.
- Erbio.
Solución:
El mercurio es el único elemento metálico que se encuentra en estado líquido en la naturaleza. Tiene efectos tóxicos en el ser humano cuando entra en contacto con la piel y mucosas. Se utiliza como método de explotación minera de bajo costo, lo que genera una grave contaminación de las aguas y el ambiente en general.
Respuesta correcta opción C.
Reactivo 64
El enlace que se establece entre el potasio y el bromo en el compuesto KBr (bromuro de potasio) es:
- Covalente.
- Covalente coordinado.
- Covalente iónico.
- Iónico.
Solución:
El bromuro de potasio es una sal formada por el catión K+ y el anión Br- unidos por enlace iónico.
Respuesta correcta opción D.
Reactivo 65
Las reacciones redox exotérmicas que ocurren por una oxidación muy rápida de uno de los elementos presentes en la reacción liberando mucha energía se conocen con el nombre de:
- Electrólisis.
- Fotólisis.
- Combustión.
- Comburente.
Solución:
La combustión es una reacción redox altamente exotérmica que ocurre por una oxidación muy rápida de uno de los elementos reaccionantes. Por ejemplo, la reacción de un alcano con un comburente que cursa durante el funcionamiento de un motor o en un horno cuando se utiliza el gas natural como combustible, en presencia de oxígeno se libera gran cantidad de calor, dióxido de carbono y agua en estado gaseoso.
Respuesta correcta opción C.
Reactivo 66
En la siguiente reacción, indique los coeficientes que faltan para que la reacción esté balanceada y se cumpla la ley de Lavoisier:
\_\_\_\_\_KCl{O}_{3}\to \_\_\_\_\_KCl+\_\_\_\_\_{O}_{2}
- 2, 1, 2
- 2, 2, 2
- 2, 2, 3
- 1, 2, 3
Solución:
Analicemos la cantidad de átomos a ambos lados de la ecuación sin balancear:
KCl{O}_{3}\to KCl+{O}_{2}

Ajustamos la cantidad de átomos de oxígeno con los siguientes coeficientes:
2 KCl{O}_{3}\to 2 KCl+3 {O}_{2}

Respuesta correcta opción C.
Reactivo 67
El número de oxidación para los elementos del grupo AI de la tabla periódica es:
- +1
- -1
- +2
- +3
Solución:
Grupo IA o familia de los metales alcalinos: H, Li, Na, K, Rb, Cs y Fr. Todos utilizan el número de oxidación +1. Aunque la ubicación del hidrógeno en el grupo IA no es real, ya que por ser gaseoso y sus otras características no puede considerarse un metal alcalino.
Respuesta correcta opción A.
Reactivo 68
Una muestra de sal de 69 g de KBr contiene una cantidad de K de 39 g y de Br de 30 g respectivamente. Calcular la composición centesimal del K presente en la sal:
- 56.5 %
- 34,3 %
- 58 %
- 63 %
Solución:
Para conocer la composición centesimal del potasio, presente en el bromuro de potasio dividimos la masa del K entre la masa general del compuesto y el resultado se multiplica por 100:
\%K= \frac{39 g }{69 g}\times 100=56.5
\%K=56.5
Respuesta correcta opción A.
Reactivo 69
Todos los enlaces sencillos de los compuestos orgánicos son _____________, y cada enlace doble o triple contiene un enlace de este tipo, por lo tanto, son los más comunes entre los compuestos orgánicos.
- Enlaces pi.
- Enlaces iónicos.
- Puentes de hidrógeno.
- Enlaces sigma.
Solución:
Todos los enlaces sencillos de los compuestos orgánicos son enlaces sigma, y cada enlace doble o triple contiene un enlace de este tipo, por lo tanto, son los más comunes entre los compuestos orgánicos
Respuesta correcta opción D.
Reactivo 70
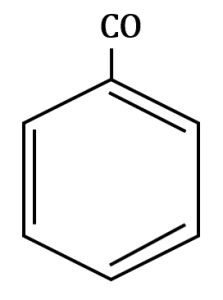
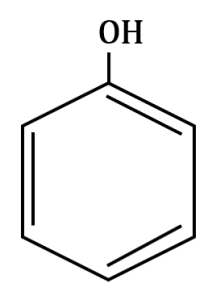
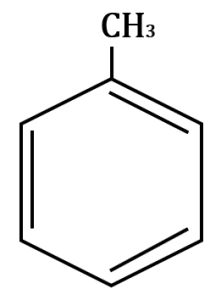
Seleccione el compuesto benzaldehído:
Solución:
El compuesto benzaldehído contiene un anillo bencénico y el grupo funcional aldehído R-CHO como lo demuestra la siguiente estructura:
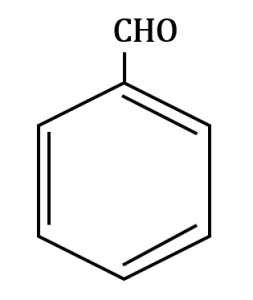
Respuesta correcta opción A.
Reactivo 71
La ______________ describe la relación entre cantidad y volumen de los gases ideales, en el cual, volúmenes iguales de gases contienen el mismo número de moléculas (a igual P y T).
- Ley de Dalton.
- Ley de Boyle.
- Ley de Lavoisier.
- Ley de Avogadro.
Solución:
La ley de Avogadro describe la relación entre cantidad y volumen de los gases ideales, en el cual, volúmenes iguales de gases contienen el mismo número de moléculas (a igual P y T).
Respuesta correcta opción D.
Reactivo 72
Cuando la concentración de una solución se expresa en N° de moles del soluto disueltos en un Kg de disolvente se habla de:
- Molaridad.
- Molalidad.
- Fracción molar.
- Nomalidad.
Solución:
Como el volumen de una disolución pude variar a diferentes condiciones de presión y temperatura, muchos investigadores utilizan la molalidad como unidad de concentración, ya que al no tomar en cuanta el volumen sino los Kg de solvente la cuantificación de las sustancias es más precisa. La molalidad se expresa en número de moles del soluto disueltos en un kilogramo de disolvente.
m= \frac{N° de moles del soluto}{Kg del disolvente}
Respuesta correcta opción B.
Reactivo 73
En la mayoría de los casos se produce un aumento de la solubilidad de una solución con el aumento de la __________________.
- Temperatura.
- Presión.
- Densidad.
- Concentración.
Solución:
En la mayoría de los casos se produce un aumento de la solubilidad de una solución con el aumento de la temperatura. Por ejemplo, cuando queremos disolver el azúcar en el café, esta se disolverá con mayor rapidez cuando la disolución está caliente, en contraste, toma más tiempo disolver el azúcar en una bebida de frutas naturales preparada con agua fría.
Respuesta correcta opción A.
Reactivo 74
¿Qué compuestos pueden separarse por descomposición electrolítica?
- Agua y cloruro de sodio.
- Cloruro de sodio y magnesio.
- Agua y oxígeno molecular.
- Cloruro de sodio y mercurio.
Solución:
El flujo de corriente a través de una disolución puede provocar la descomposición de las sustancias disueltas en ella. Por ejemplo, la electrólisis del agua la descompone en hidrógeno y oxígeno o la electrólisis de una sal como el NaCl, la cual se separa en sus iones constituyentes Na+ y Cl-.
Respuesta correcta opción A.
Reactivo 75
En las celdas galvánicas en el cátodo se lleva a cabo la _________ del cobre y en el ánodo se realiza la _________ del zinc.
- Oxidación – reducción.
- Oxidación – descomposición.
- Reducción – oxidación.
- Descomposición – reducción.
Solución:
Las celdas galvánicas son dispositivos que generan electricidad a través de reacciones de óxido reducción. El principio de su funcionamiento se basa en la oxidación del electrodo de zinc (ánodo) Zn \to Z{n}^{+2}+2{e}^{-} sumergido en una disolución de sulfato de zinc. Y la reducción del electrodo de cobre (cátodo) C{u}^{+2}+2{e}^{-}\to Cu sumergido en una disolución de sulfato de cobre.
Ambos procesos son reacciones de semicelda en donde hay transferencia de electrones mediante un conductor externo.
Respuesta correcta opción C,