Segunda parte de nuestro examen simulador de química para carreras del área de Ingenierías y ciencias físico matemáticas. En esta ocasión, vamos a resolver los ejercicios del 11 al 20.

Continuaremos con nuestro enfoque práctico y directo, presentándote problemas variados que desafiarán tu comprensión y agilidad en la materia.
Este bloque está diseñado para consolidar lo aprendido anteriormente y para introducirte en nuevos temas que son vitales para ganar algunos puntos en el examen.
Al igual que en la primera parte, te acompañaremos en cada paso, asegurándonos de que cada solución sea comprensible y que puedas aplicar estos métodos por tu cuenta el día del examen real.
Reactivo 11
Los compuestos con _____________ suelen ser sólidos a temperatura ambiente, cristalinos, solubles en agua y con puntos de fusión elevados.
- Enlace covalente coordinado.
- Enlace simple.
- Enlace iónico.
- Enlace metálico.
Solución:
El enlace iónico es la unión química que se genera mediante una transferencia de electrones entre los átomos que participan. Uno de ellos cede los electrones mientras el otro los acepta, generando un anión y un catión que permanecen en estrecha unión por las fuerzas de atracción eléctrica.
En este sentido, las características de los compuestos iónicos es que suelen ser sólidos cristalinos a temperatura ambiente, con elevados puntos de fusión y ebullición. En soluciones acuosas se separan en sus iones constituyentes y permiten el paso de la corriente.
Con base en la justificación teórica, se concluye que:
Los compuestos con enlace iónico suelen ser sólidos a temperatura ambiente, cristalinos, solubles en agua y con puntos de fusión elevados. Siendo la respuesta correcta la opción C.
Reactivo 12
Seleccione los números de oxidación correspondientes para el Mg y el H en reactivos y productos, en la siguiente reacción redox:
M{g}_{\left(s\right)}+2HC{l}_{\left(ac\right)} \to MgC{l}_{2 \left(ac\right)}+{H}_{2}\uparrow- +2, +4, 0, 8
- 0, +1, +2, 0
- +2, 0, -1, 0
- 0, -1, +1, +2
Solución:
Las reacciones redox se caracterizan por la transferencia de electrones de una sustancia a otra, en la reacción del enunciado la transferencia ocurre de la siguiente manera:
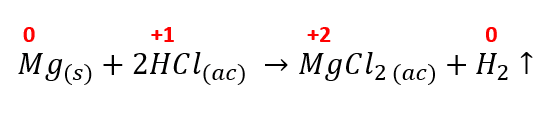
Recordemos que cuando el elemento se encuentra sin combinar, el número de oxidación es cero, como es el caso del magnesio y el hidrógeno gaseoso.
La respuesta correcta es la opción B.
Reactivo 13
Indicar la reacción química que cumple con la ley de conservación de la masa:
- Fe+S \to FeS
- 4Fe+{O}_{2} \to Fe{O}_{3}
- 4Fe+3{O}_{2}\to FeO
- 2Fe+S \to FeS{O}_{3}
Solución:
Con base en la teoría atómica y la ley de conservación de la masa propuesta por Lavoisier, los átomos (o la materia) no se crean ni se destruyen, solo se transforman, es decir que en las reacciones químicas la cantidad de reactante debe ser igual a la cantidad de producto, pero con un ordenamiento diferente.
El balanceo de una ecuación pone de manifiesto el cumplimiento de la ley, lo que nos sirve de guía para evaluar las reacciones que presenta el enunciado.
En donde se observa que las reacciones 4Fe+{O}_{2} \to Fe{O}_{3} y 4Fe+3{O}_{2}\to FeO no cumplen con la ley de Lavoisier. La reacción 2Fe+S \to FeS{O}_{3} tampoco se ajusta a las condiciones de conservación de la masa, porque en los productos, incluso hay un átomo que no existe en los reactantes.
Por lo tanto, la reacción Fe+S \to FeS es la única que cumple con la ley de conservación de la masa, en la que existe la misma cantidad de átomos a ambos lados de la reacción.
La respuesta correcta es la opción A.
Reactivo 14
Un proceso_________ transfiere calor del sistema a los alrededores y produce un incremento en la__________ de los alrededores.
- Endotérmico – entalpía.
- Endotérmico – entropía.
- Exotérmico – entalpía.
- Exotérmico – entropía.
Solución:
Cuando se realiza un proceso exotérmico en un sistema determinado, el calor liberado que se transfiere a los alrededores incrementa el movimiento de las moléculas cercanas. Como resultado existe un incremento de la entropía de las adyacencias.
Por lo tanto, un proceso exotérmico transfiere calor del sistema a los alrededores y produce un incremento en la entropía de los alrededores.
La respuesta correcta es la opción D.
Reactivo 15
Determinar el número de moles de oxígeno que se requieren para la combustión de 12 moles de gas metano.
{CH}_{4}+{O}_{2} \to C{O}_{2}+{H}_{2}O
- 12
- 24
- 32
- 48
Solución:
Lo primero que se debe hacer es balancear la ecuación:
{CH}_{4}+{O}_{2} \to C{O}_{2}+{H}_{2}O
Ecuación balanceada:
{CH}_{4}+2{O}_{2} \to C{O}_{2}+2{H}_{2}O
Con base en la ecuación se deduce que con 2 moles de {O}_{2} se produce la combustión de 1 mol de gas metano ¿Cuántos moles de oxígeno serán necesarios para producir la combustión de 12 moles de gas metano?
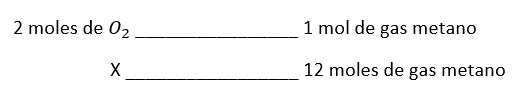
La relación matemática es la siguiente:
12 mol metano \times \frac{{2 mol O}_{2}}{1 mol metano}=24 mol de {O}_{2}
Se necesitan 24 moles de oxígeno para producir la combustión de 12 moles de gas metano.
Respuesta correcta opción B.
Reactivo 16:
Las _________________ descomponen moléculas mediante el uso de la electricidad.
- Termoquímica.
- Celdas electrolíticas.
- Sustancias catalíticas.
- Enzimas.
Solución:
Algunos compuestos pueden ser separados en sus átomos constituyentes cuando son sometidos a electricidad, como por ejemplo el agua y el cloruro de sodio. Es lo que sucede con el uso de celdas electrolíticas. Respuesta correcta opción B.
Reactivo 17
Las relaciones de presión y volumen de los gases ideales se rigen, principalmente, por la ____________ en donde el volumen es inversamente proporcional a la presión.
- Ley de Charles.
- Ley de Avogadro.
- Ley de Gay-Lussac.
- Ley de Boyle.
Solución:
Las relaciones de presión y volumen de los gases ideales se rigen, principalmente, por la ley de Boyle en donde el volumen es inversamente proporcional a la presión a un valor de temperatura y n (número de moles) constantes. En su ley se explica que si la presión de un gas aumenta el volumen disminuye y si la presión disminuye, el volumen del gas aumenta.
La respuesta correcta es la opción D.
Reactivo 18
En todos los cálculos que se realizan de las leyes de los gases, la temperatura debe ser expresada en kelvins. Esta escala toma como 0 K al cero absoluto, el cual tiene un valor de ___________ en grados Celsius.
- – 273.15
- – 1
- 0
- – 215. 73
Solución:
En química y otras ciencias, cuando se amerita aplicar cálculos basados en las leyes de los gases, la temperatura obligatoriamente debe ser expresada en kelvins, el cero absoluto expresado en grados Celsius tiene un valor de – 273.15 °C.
La respuesta correcta es la opción A.
Reactivo 19
Durante el curso de una reacción redox, de forma global, los electrones fluyen del __________ al ____________ porque existe una diferencia de energía potencial eléctrica entre los electrodos.
- Ánodo – iones.
- Cátodo – ánodo.
- Iones – cátodo.
- Ánodo – cátodo.
Solución:
Durante el curso de la reacción redox, los electrones fluyen externamente desde el ánodo hacia el cátodo. La diferencia de energía potencial que existe entre los electrodos se puede medir con el uso de un voltímetro. En este sentido, se puede determinar que la respuesta correcta es la opción D.
Reactivo 20
La ____________ es la rama de la química que estudia los aspectos tridimensionales de las moléculas.
- Estequiometría.
- Polarización.
- Cinética.
- Estereoquímica.
Solución:
La estereoquímica es la rama de la química que estudia los aspectos tridimensionales de las moléculas. La estructura tridimensional de una molécula supone una importancia marcada, ya que al conocerla se pueden determinar las propiedades de una molécula o su comportamiento biológico.
Respuesta correcta opción D.

