Hemos llegado a la última parte de nuestra megaguía de ejercicios resueltos del Exani II en el módulo de Química. Por eso, si queremos reconocer tu esfuerzo. Además, si acabas de llegar y quieres ver las partes anteriores de esta guía, aquí abajo tienes el link directo. Sin más que decir, aquí te dejamos los detalles.

Acá te mostramos los detalles más relevantes referentes al Exani II:
- Desarrollo: Ceneval
- Examen de admisión: Exani II
- Reactivos: 168
- Tipo: Opción múltiple
- Duración: 4 horas y media
- Modalidades: Presencial, en línea y desde casa.
Estructura del Exani II
Vamos a desarrollar los ejercicios de la guía de Química del Exani II. Pero antes, queremos aclarar cuál es la estructura general de esta prueba.
Para ello, acá te dejamos una tabla donde desglosamos todos los elementos del Exani II:
| Área | Reactivos |
|---|---|
| Habilidades y conocimientos | |
| Pensamiento matemático | 30 |
| Comprensión lectora | 30 |
| Redacción indirecta | 30 |
| Módulos de conocimientos específicos | |
| Módulo 1 | 24 |
| Módulo 2 | 24 |
| Subtotal de reactivos | 138 |
| Diagnóstico | |
| Inglés | 30 |
| Total de reactivos | 168 |
Temario Química
El módulo de Química es uno de los correspondientes al área de Conocimiento Específico, por lo que aparecerá solamente en carreras donde la institución considere que esta es una de las áreas de estudio fundamentales para ingresar a la carrera.
Dicho esto, aquí desglosamos todos los temas que se abordan en este módulo:
- Fundamentos generales
- Tipos de enlaces químicos (ejemplos y diferencia numérica de electronegatividad)
- Tipos, porcentaje, partes por millón y molaridad de soluciones
- Tipos de reacciones químicas en ecuaciones balanceadas
- Coeficientes de reactivos y productos
- Ecuaciones químicas que resultan de situaciones o experimentos científicos
- Átomos de elementos y compuestos en ecuaciones químicas
- Relación estequiométrica entre reactivos y compuestos
- Gramos y moles de reactivos y productos
- Ejemplos de procesos endotérmicos y exotérmicos
- Valor de entalpía de reacciones químicas de síntesis y combustión
- Constante de equilibrio
- Química orgánica
- Propiedades e hibridación del átomo de carbono
- Estructura lineal y geometría de alcanos, alquenos y alquinos
- Reglas de la nomenclatura IUPAC para estructuras de hidrocarburos y compuestos orgánicos
- Estructura y descripción de grupos funcionales
- Nombre y estructura de carbohidratos y aminoácidos
- Estructura de los enlaces glucosídico y peptídico
Ejercicio 41: Reactivos nucleofílicos
Relaciona el nombre de los siguientes reactivos nucleofílicos con su fórmula correspondiente:
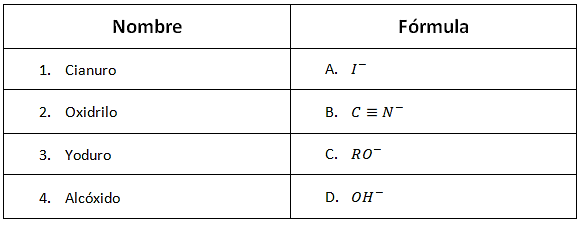
- 1B, 2D, 3A, 4C
- 1A, 2B, 4D, 3C
- 1D, 2C, 3B, 4A
- 1C, 2A, 3B, 4D
Solución:
Los reactivos nucleofílicos pueden ser aniones o pueden ser moléculas neutras, su rasgo fundamental es que poseen exceso de electrones. La relación queda establecida de la siguiente manera:
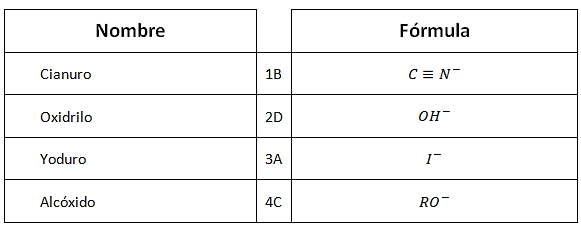
Por lo tanto, la opción correcta es la A.
Ejercicio 42: Soluciones
Una disolución es una mezcla homogénea de dos o más sustancias y cuando la cantidad de soluto es superior a la que puede disolver el disolvente se dice que la disolución está:
- Saturada
- Diluida
- Concentrada
- Sobresaturada
Solución:
Una disolución es una mezcla homogénea de dos o más sustancias y cuando la cantidad de soluto es superior a la que puede disolver el disolvente se dice que la disolución está sobresaturada.
Por el contrario, una disolución saturada contiene la máxima cantidad de soluto que se disuelve en un disolvente específico. Las disoluciones insaturadas son aquellas en las que la cantidad de soluto es inferior a la capacidad de dilución que tiene el disolvente utilizado.
La respuesta correcta es la opción D.
Ejercicio 43: Reacciones químicas
¿Qué productos se forman a partir de los siguientes reactantes durante una reacción química?
\mathrm{Cu}(\mathrm{OH})_{2}+\mathrm{H}_{2} \mathrm{SO}_{4} \rightarrow
- \mathrm{Cr}(\mathrm{OH})_{3}
- \mathrm{CuH}+\mathrm{H}_{2} \mathrm{O}
- \mathrm{KOH}+\mathrm{H}_{2} \mathrm{O}
- \mathrm{CuSO}_{4}+2 \mathrm{H}_{2} \mathrm{O}
Solución:
Debemos conocer los reactantes para predecir cómo se comportan y qué producto originan. El \mathrm{Cu}(\mathrm{OH})_{2} es una base, se puede identificar por la presencia del grupo hidroxilo y el \mathrm{H}_{2} \mathrm{SO}_{4} es un ácido que se reconoce por el H al principio del compuesto.
En este sentido estamos en presencia de una reacción química de neutralización, en la que al combinar un ácido y una base se anula el efecto mutuo de dichas sustancias y el producto formado es sal y agua.
La ecuación general de este tipo de reacciones es la siguiente:
\text { Hidróxido }+\text { Ácido } \rightarrow \text { Sal }+\text { Agua }
\mathrm{Cu}(\mathrm{OH})_{2}+\mathrm{H}_{2} \mathrm{SO}_{4} \rightarrow \mathrm{sal}+\text { agua }
Entre las opciones que ofrece el enunciado, la que corresponde al producto de la reacción es la D. Allí se pueden visualizar todos los elementos que participan entre los reactantes y cómo sufren un cambio durante la reacción, cumpliendo la ley de conservación de la masa.
\mathrm{Cu}(\mathrm{OH})_{2}+\mathrm{H}_{2} \mathrm{SO}_{4} \rightarrow \mathrm{CuSO}_{4}+2 \mathrm{H}_{2} \mathrm{O}
Presencia de la formación de la sal: \mathrm{CuSO}_{4} y agua \left(\mathrm{H}_{2} \mathrm{O}\right) .
La respuesta correcta es la opción D.
Ejercicio 44: Compuestos químicos
¿Cuál es la diferencia entre una sal haloidea y oxisal?
- Presencia de H y ausencia de H
- Ausencia de H y presencia de H
- Ausencia de O y presencia de O
- Presencia de O y ausencia de O
Solución:
Las sales haloideas no contienen oxígeno y una oxisal si contiene oxígeno. Por ejemplo: el KCl corresponde a una sal haloidea y se observa la ausencia de oxígenos en la sal. Por el contrario, el \mathrm{Ba}\left(\mathrm{NO}_{3}\right) 2 es una oxisal en donde sí hay presencia de átomos de oxígeno.
La respuesta correcta es la opción C.
Ejercicio 45: Símbolos de los elementos
Los símbolos Ne, Sc, Rb y Pt corresponden a los elementos:
- Neón, escandio, rubidio, platino
- Níquel, estroncio, rubidio, plata
- Azufre, estroncio, rubidio, plata
- Neón, estroncio, rubidio, plata
Solución:
La simbología química se considera un pilar fundamental para comprender las reacciones y los elementos que participan en ella. Los símbolos de los elementos, establecidos por la IUPAC, siempre se escriben con la primera letra en mayúscula. Este último detalle se debe tener presente en todo momento porque si se escribe un elemento con ambas letras en minúsculas, lo escrito no representará el elemento en cuestión.
Los símbolos se corresponden de la siguiente manera:
- Ne: neón
- Sc: escandio
- Rb: rubidio
- Pt: platino
La respuesta es la opción A.
Ejercicio 46: Propiedades coligativas
El _______ __ ___________ se define como la temperatura en la cual la presión de vapor de un material líquido iguala a la presión atmosférica.
- Punto de fusión
- Punto de ebullición
- Punto de congelación
- Aumento de la presión osmótica
Solución:
El punto de ebullición se define como la temperatura en la cual la presión de vapor de un material líquido se iguala a la presión atmosférica.
Un líquido se considera en su punto de ebullición cuando la velocidad de evaporación ha superado en su totalidad la condensación, y para ello ha tenido que vencer todas las fuerzas que se oponen, como la presión atmosférica.
En base a la teoría la respuesta correcta es la opción B.
Ejercicio 47: Equilibrio iónico
El agua pura tiene un pH=7 por lo tanto es un líquido:
- Ácido
- Básico
- Neutro
- Alcaloide
Solución:
La escala de pH se encuentra entre el siguiente rango:
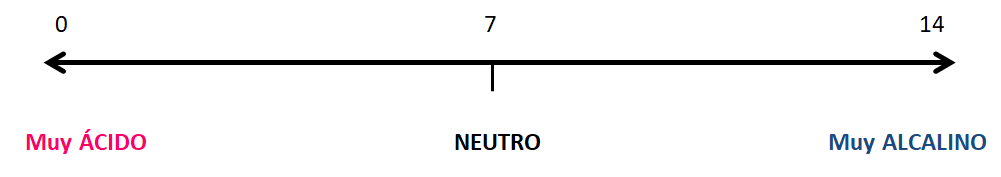
El agua pura, al tener un pH=7 es un líquido neutro.
La respuesta correcta es la opción C.
Ejercicio 48: Compuestos orgánicos, alquenos
Los alquenos se conocen como hidrocarburos insaturados, un antiguo nombre de esta familia de compuestos (que se utiliza todavía con frecuencia) es:
- Alcanos
- Olefinas
- Cetonas
- Alquinos
Solución:
Al analizar cada una de las opciones, nos damos cuenta que la A, la C y la D no corresponden a la respuesta correcta del enunciado, porque cada una de ellas es una familia distinta de compuestos orgánicos. En ese sentido la respuesta correcta es la opción B.
En efecto, los alquenos son llamados hidrocarburos insaturados u olefinas, del latín óleum (aceite) y facere (hacer). Estos compuestos poseen un doble enlace en su cadena carbonada entre dos carbonos consecutivos (C=C) este enlace está formado por un enlace sigma (estable) y un enlace pi perpendicular al enlace sigma. El doble enlace es el que determina las propiedades de los alquenos.
Ejercicio 49: Compuestos aromáticos
La fórmula C_{6} H_{6} corresponde al _____________.
- Tolueno
- Etileno
- Benceno
- Xileno
Solución:
El benceno es el primer miembro de una serie de hidrocarburos llamados hidrocarburos aromáticos. Fue descubierto por Michael Faraday y su fórmula molecular es \mathrm{C}_{6} \mathrm{H}_{6} . El benceno es un líquido a temperatura ambiente, incoloro, insoluble en agua y soluble en solventes orgánicos no polares.
En base a la teoría, la respuesta correcta es la opción C.
Ejercicio 50: Compuestos orgánicos
El eteno es el único hidrocarburo, que se conoce hasta ahora, que tiene efectos nocivos adversos sobre la vegetación a concentraciones ambientales de 1 ppm aproximadamente e incluso menos ¿A qué grupo funcional pertenece dicho compuesto?
- Alcanos
- Alquinos
- Alquenos
- Hidrocarburo saturado
Solución:
El eteno pertenece al grupo de los alquenos y se puede identificar debido al sufijo –eno que corresponde a la nomenclatura de este tipo de hidrocarburos insaturados.
La respuesta correcta es la opción C.

