Resuelve la cuarta parte del examen simulador de química del área de las Ciencias Médico Biológicas. Ahora vamos con los ejercicios del 46 al 60.

¡Felicidades! Ya casi terminas la serie de exámenes simulacro de química para el área de CMB. Sigue aprendiendo con nuestra ayuda hasta llegar a la meta.
El penúltimo simulacro de química te demuestra todos los conocimientos que has reforzado en tu paso por cada reactivo y que en definitiva tus tiempos de respuesta cada vez son mejores ¡No te detengas!
Reactivo 46
Si se desea separar una mezcla de aceites esenciales para aislar la sustancia de interés, ¿Qué método de separación de mezclas debo utilizar?
- Destilación.
- Decantación.
- Filtración.
- Centrifugación.
Solución:
El enunciado ejemplifica una situación de la vida real en la que se necesita aplicar una técnica experimental con base en los conocimientos previos de los métodos de separación de mezclas, como se mencionó con anterioridad es muy común este tipo de reactivos en el IPN.
El concepto de destilación nos dice que es una técnica para separar dos líquidos miscibles entre sí con diferentes puntos de ebullición. Amerita la aplicación de procesos físicos como la evaporación y la condensación.
Como es una mezcla de aceites esenciales, es decir, su naturaleza química es la misma, son líquidos miscibles entre sí, por lo que se debe destilar la sustancia para separar el analito de interés.
Respuesta correcta opción A.
Reactivo 47
La principal característica de la estructura del siguiente compuesto es que es una molécula:
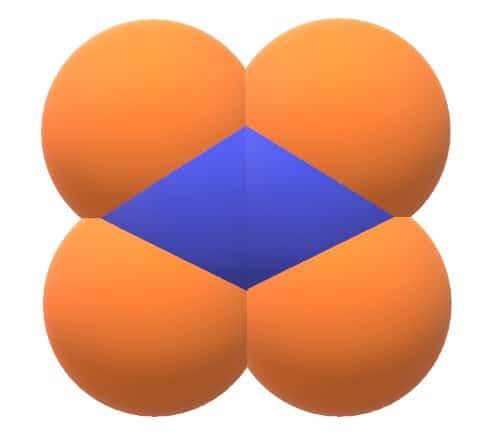
- Diatómica
- Saturada
- Poliatómica
- Monoatómica
Solución:
La estructura pertenece a una molécula poliatómica. En ella se pueden observar diferentes átomos enlazados entre sí en una representación tridimensional.
Respuesta correcta opción C.
Reactivo 48
Selecciones los elementos metaloides, es decir, aquellos que poseen un comportamiento con características de los elementos metálicos y no metálicos:
- In
- Cd
- B
- Si
- Se
- 1, 2, 3
- 1, 4, 5
- 2, 3, 4
- 3, 4, 5
Solución:
Los metaloides o semimetales son elementos con características metálicas y no metálicas. Se utilizan, en su gran mayoría, para la fabricación de componentes electrónicos y dispositivos semiconductores como diodos, transistores, compuertas lógicas, rectificadores controlados, fotorresistores, entre otros.
El silicio es el corazón de todos los dispositivos semiconductores mencionados, pero por si solo no les atribuye todas sus características. Este se expone a un proceso químico de dopado en el que se le inyectan impurezas aceptoras o donadoras de electrones, para formar material semiconductor tipo P o tipo N, que modifican su conductividad y permiten el transporte de electricidad en función del voltaje aplicado en sus terminales.
Otros de los elementos que conforman este grupo son:
- Boro
- Germanio
- Antimonio
- Arsénico
- Telurio
- Polonio
Respuesta correcta opción D.
Reactivo 49
La estructura de Lewis representa una molécula de amoníaco, la cual presenta enlaces:
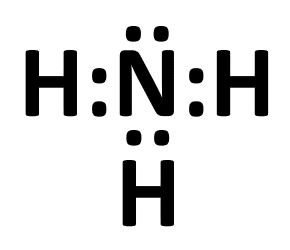
- Iónico.
- Coodinado.
- Covalente.
- Interacciones electrostáticas.
Solución:
Durante las reacciones químicas los átomos interactúan entre sí para formar moléculas y compuestos. En el proceso se genera una fuerza de atracción que los mantiene unidos, el enlace químico. Los electrones de la parte más externa del átomo, es decir, los que pertenecen a la capa de valencia son los encargados de establecer el enlace.
Los símbolos de Lewis representan los electrones de valencia que participan en la formación del enlace químico. Esto permite asegurar que la cantidad total de electrones no varía durante la reacción química.
La estructura de Lewis que brinda el enunciado corresponde a la molécula de amoniaco. Sus átomos se mantienen juntos mediante enlaces covalentes, el cual es la unión entre dos o más átomos que comparten uno o más pares de electrones.
Respuesta correcta opción C.
Reactivo 50
En las reacciones redox una semirreacción muestra explícitamente:
- Los electrones transferidos.
- El agente reductor.
- El agente oxidante.
- El elemento que se reduce.
Solución:
En el proceso de reacciones redox se visualizan dos etapas, una implica la pérdida de electrones, y otra la ganancia de los mismos, lo que se conoce como semirreacción. Y la suma de ambas ejemplifica la reacción global.
Por ejemplo, el compuesto iónico conocido como óxido de magnesio, formado por los iones M{g}^{2+} y {O}^{2-}
2Mg+ {O}_{2} \to 2MgO
La transferencia electrónica se visualiza en dos etapas:
- Los dos átomos de Mg pierden cuatro electrones y se los ceden al oxígeno, a través de la semirreacción: 2Mg\to 2M{g}^{2+}+4{e}^{-}
- El oxígeno molecular gana cuatro electrones, la semirreacción es: {O}_{2}+4{e}^{-}\to 2{O}^{2-}
Respuesta correcta opción A.
Reactivo 51
Un ejemplo de conservación de la masa en la naturaleza se evidencia en ___________________, lo que indica que la naturaleza no produce materia, sino que simplemente se transforma.
- Los ciclos biogeoquímicos.
- Las reacciones redox.
- Las celdas galvánicas.
- Los gases ideales.
Solución:
La materia circula en numerosos procesos que forman parte de los ecosistemas. Se mueve a través de los organismos como lo indica la cadena alimentaria, pasa de organismos vivos al ambiente inerte (factor abiótico) y de regreso. Es decir, cumple un ciclo que integra las interacciones biológicas, químicas y geológicas lo que se conoce como ciclos biogeoquímicos.
La materia no puede ser fabricada de nuevo ni escapar de nuestro planeta, la ley de conservación de la masa lo respalda. Por ello, en términos generales la materia es reciclada dentro y entre los ecosistemas.
Respuesta correcta opción A.
Reactivo 52
La siguiente semirreacción del hierro indica que:
Fe \to F{e}^{+2}+2{e}^{-}
- Gana electrones.
- Se reduce.
- Se oxida.
- No se altera.
Solución:
La semirreacción Fe \to F{e}^{+2}+2{e}^{-} indica la pérdida de electrones del hierro. Es una semirreacción de oxidación.
Respuesta correcta opción C.
Reactivo 53
La __________________ indica el por porcentaje en masa de cada elemento que participa en un compuesto químico.
- Composición centesimal.
- Porcentaje masa/masa.
- Porcentaje volumen/volumen.
- Porcentaje masa/volumen.
Solución:
La composición centesimal indica el porcentaje en masa de cada elemento que participa en un compuesto químico. Para calcularla se divide la masa atómica del elemento entre el peso molecular de la sustancia y se multiplica el valor por 100.
\frac{Masa atómica del elemento}{PM de la sustancia}\times 100
Respuesta correcta opción A.
Reactivo 54
Cuando los orbitales de un mismo átomo interactúan entre sí ¿Qué tipo de orbitales se generan?
- Orbitales moleculares.
- Orbitales descentralizados.
- Orbitales antienlaces.
- Orbitales atómicos híbridos.
Solución:
Los orbitales atómicos híbridos son el resultado de la mezcla de orbitales de un mismo átomo. La geometría que adoptan los estos orbitales sirven para explicar los ángulos de enlace y las estructuras reales de los compuestos orgánicos.
Respuesta correcta opción D.
Reactivo 55
Identifique el nombre del siguiente compuesto:
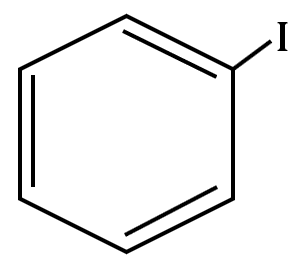
- Anilina.
- Yoduro.
- Yodobenceno.
- Yodotolueno.
Solución:
La estructura de la molécula nos indica que se trata de un benceno, por la disposición de los dobles enlaces. Unido al anillo bencénico se encuentra un halógeno, el yodo. La nomenclatura para la estructura es: yodobenceno.
Respuesta correcta opción C.
Reactivo 56
La ___________ indica que dos gases se mezclan progresivamente entre sí, mientras que la ____________ explica que las moléculas de gas atraviesan orificios con diámetros muy pequeños cuando se someten a presión.
- Efusión – atracción.
- Difusión – expansión.
- Repulsión – efusión.
- Difusión – efusión.
Solución:
La difusión indica que dos gases se mezclan progresivamente entre sí, mientras que la efusión explica que las moléculas de gas atraviesan orificios con diámetros muy pequeños cuando se someten a presión.
Respuesta correcta opción D.
Reactivo 57
¿Cuál es la concentración porcentual de una sustancia que expresa la masa en gramos de soluto disuelta en 100 ml disolución?
- %m/m
- %v/v
- %estándar
- %m/v
Solución:
La concentración porcentual que relaciona la masa y el volumen de una sustancia es el %m/v.
Respuesta correcta opción D.
Reactivo 58
Los refrescos gaseosos tienen disuelto dióxido de carbono en un líquido, por lo tanto, son un tipo de disolución:
- Gas – gas.
- Liquido – gas.
- Gas – sólido.
- Líquido – líquido.
Solución:
Los refrescos gaseosos son una disolución formada por líquido y gas.
Respuesta correcta opción B.
Reactivo 59
Todas las reacciones electroquímicas implican la transferencia de electrones y, por lo tanto, son:
- Reacciones redox.
- Reacciones de síntesis.
- Reacciones de descomposición.
- Reacciones de doble desplazamiento.
Solución:
Las reacciones electroquímicas se fundamentan en que la energía liberada por una reacción que ocurre espontáneamente se transforma en energía eléctrica o la electricidad producida se utiliza para producir una reacción que requiere energía. Todo ello se basa en reacciones redox (transferencia de electrones).
Respuesta correcta opción A.
Reactivo 60
La fuerza electromotriz de una celda es:
- La diferencia de voltaje generada en toda la celda.
- La diferencia de potencial entre los dos electrodos.
- El viaje de los electrones hacia el cátodo.
- La cantidad de voltaje generado en la semicelda.
Solución:
La fuerza electromotriz de una celda es la diferencia de potencial entre los dos electrodos. El voltaje de una celda, además de la naturaleza de los iones y los electrodos, también depende de la concentración iónica y temperatura óptima de funcionamiento de la celda.
Respuesta correcta opción B.

