Para continuar con tu preparación de cara a presentar el Exani II, estás invitado a estudiar junto a nosotros con esta tercera parte de una guía resuelta de reactivos de Química. Ten presente que si aún no has checado las partes anteriores de esta guía, aquí abajo encontrarás los enlaces para llegar a ellos. Sin más que añadir ¡Comenzamos!

Puedes dar un vistazo a los detalles destacados del Exani aquí:
- Desarrollo: Ceneval
- Examen de admisión: Exani II
- Reactivos: 168
- Tipo: Opción múltiple
- Duración: 4 horas y media
- Modalidades: Presencial, en línea y desde casa.
Estructura del Exani II
Queremos dar inicio a la resolución de ejercicios de esta guía de Química. No obstante, vale la pena dedicar unos segundos a ver cómo es la estructura del Exani II.
Ya aclarado este punto, acá tienes un desglose con los aspectos claves que debes tener en consideración:
| Área | Reactivos |
|---|---|
| Habilidades y conocimientos | |
| Pensamiento matemático | 30 |
| Comprensión lectora | 30 |
| Redacción indirecta | 30 |
| Módulos de conocimientos específicos | |
| Módulo 1 | 24 |
| Módulo 2 | 24 |
| Subtotal de reactivos | 138 |
| Diagnóstico | |
| Inglés | 30 |
| Total de reactivos | 168 |
Temario Química
A continuación te presentamos todos los temas que se abarcan en el módulo de conocimiento específico de Química en el Exani II:
- Fundamentos generales
- Tipos de enlaces químicos (ejemplos y diferencia numérica de electronegatividad)
- Tipos, porcentaje, partes por millón y molaridad de soluciones
- Tipos de reacciones químicas en ecuaciones balanceadas
- Coeficientes de reactivos y productos
- Ecuaciones químicas que resultan de situaciones o experimentos científicos
- Átomos de elementos y compuestos en ecuaciones químicas
- Relación estequiométrica entre reactivos y compuestos
- Gramos y moles de reactivos y productos
- Ejemplos de procesos endotérmicos y exotérmicos
- Valor de entalpía de reacciones químicas de síntesis y combustión
- Constante de equilibrio
- Química orgánica
- Propiedades e hibridación del átomo de carbono
- Estructura lineal y geometría de alcanos, alquenos y alquinos
- Reglas de la nomenclatura IUPAC para estructuras de hidrocarburos y compuestos orgánicos
- Estructura y descripción de grupos funcionales
- Nombre y estructura de carbohidratos y aminoácidos
- Estructura de los enlaces glucosídico y peptídico
Ejercicio 31: Simbología química
En las ecuaciones químicas ¿Cuál es el signo que se utiliza para indicar el movimiento de electrones dentro de una reacción química en curso?

- \Delta
- \rightarrow
- \uparrow
Solución:
Las flechas curvas son las que se utilizan para indicar el movimiento de electrones dentro de una reacción química. Por ejemplo, indican el movimiento de de un nucleófilo a un electrófilo en las reacciones orgánicas.
La respuesta correcta es la opción A.
Ejercicio 32: Derivados halogenados
Nombre el siguiente compuesto orgánico
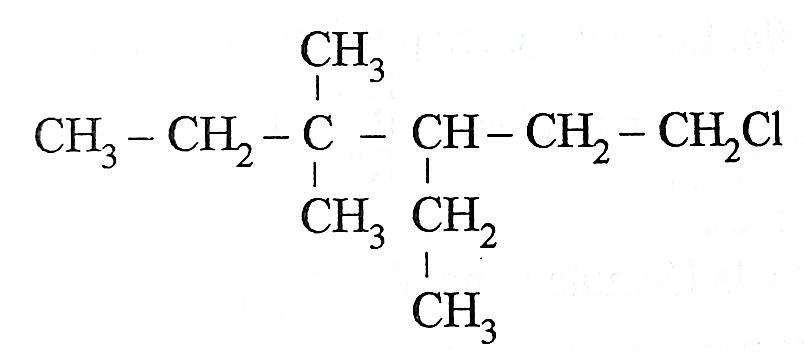
- 3,5 –terbutil –2 –etil –1– cloropentano
- 4,4 –dimetil –3 –etil –1– clorohexano
- 4,4 –terbutil –5 –etil –2 –clorobutano
- 5,6 –dimetil –7 –isobutil –5 –hexano
Solución:
- Primero reconocemos que se trata de un haluro de alquilo porque hay presencia de un halógeno (Cl) en la cadena carbonada
- Ahora se debe numerar la cadena principal (esta debe contener el halógeno)
- La numeración se inicia por el extremo derecho del compuesto
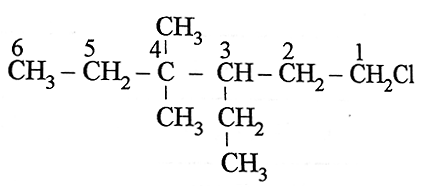
- El haluro de alquilo tiene una cadena base de 6 átomos de carbono y el Cl se encuentra en el carbono N° 1, por lo tanto se nombra: 1-clorohexano indicando la posición del halógeno
- Los grupos alquilo están ubicados en la posición 4 y en la posición 3
- En la posición 4 hay dos metil, por lo tanto será: 4,4-dimetil
- En la posición 3 hay un etil: 3-etil
El nombre del compuesto es: 4,4 –dimetil –3 –etil –1– clorohexano
La opción correcta es la B.
Ejercicio 33: Compuestos orgánicos
Los compuestos orgánicos cuyos átomos de carbono están unidos por enlaces sencillos se denominan compuestos _________, mientras que aquellos que presentan un doble o triple enlace se denominan __________.
- Alcanos – aldehídos
- Cetonas – ácidos
- Alquenos – alquinos
- Saturados – insaturados
Solución:
Los compuestos orgánicos cuyos átomos de carbono están unidos por enlaces sencillos se denominan compuestos saturados, mientras que aquellos que presentan un doble o triple enlace se denominan insaturados. Un ejemplo de compuestos saturados son los alcanos también llamados parafinas y entre los compuestos insaturados, podemos mencionar los alquenos o alquinos.
Respuesta correcta opción D.
Ejercicio 34: Compuestos orgánicos
La categoría del átomo de carbono central en la siguiente estructura, es:
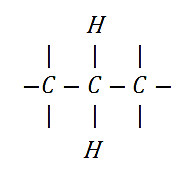
- Primario
- Secundario
- Terciario
- Alqueno
Solución:
El carbono central, es un átomo de carbono secundario porque se encuentra unido a dos átomos de carbono adicionales. Los carbonos secundarios tienen la particularidad de ser siempre intermedios, al igual que los carbonos terciarios (estos últimos unidos a tres átomos de C adicionales).
Por otro lado, los carbonos primarios, poseen sólo un enlace con otro átomo de carbono y siempre se ubican en posición terminal.
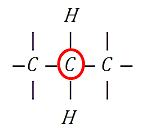
La respuesta correcta es la opción B.
Ejercicio 35: Aminas
Identifica el número con que corresponde al grupo funcional amina:
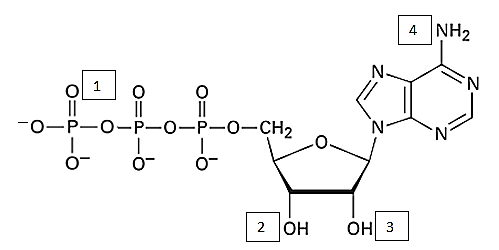
- 2
- 4
- 1
- 3
Solución:
La amina es la molécula que se encuentra señalada por el N° 4.
Las aminas R-N H_{4} se pueden considerar como derivados del amoníaco por sustitución de uno, dos o tres H por grupos alquilo (R) o arilo (Ar).
La respuesta correcta es la opción B.
Ejercicio 36: Fenoles
Aunque los alcoholes y los fenoles poseen un grupo hidroxilo (OH) los fenoles difieren de los alcoholes debido a que…
- Los fenoles tienen el grupo OH unido al anillo bencénico
- Los fenoles tienen el grupo OH unido a una cadena alifática
- Los alcoholes tienen el grupo OH al principio de su cadena carbonada
- Los alcoholes tienen el grupo OH al final de su cadena carbonada
Solución:
Los fenoles son aquellos compuestos orgánicos que poseen uno o más grupos OH unidos directamente al carbono (s) de un anillo bencénico. Los fenoles no son alcoholes, tienen muchas diferencias respecto a sus reacciones químicas a pesar de que ambos poseen el grupo hidroxilo.
Una de sus principales diferencias es, como se explicó, que los fenoles poseen el grupo OH unido al anillo bencénico. Sí por el contrario, el grupo OH se encuentra unido a una cadena alifática el compuesto es un alcohol, aun cuando dicha cadena está unida a un anillo bencénico.
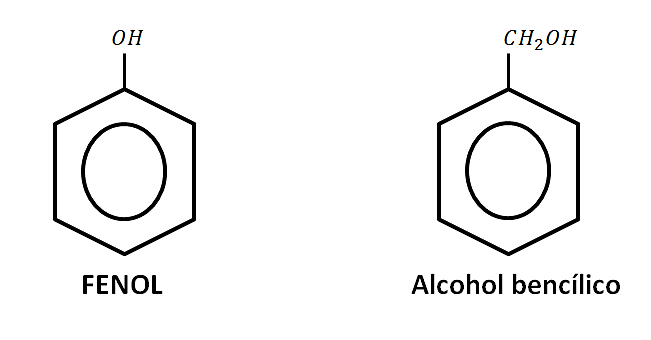
En base a la teoría, la respuesta correcta es la opción A.
Ejercicio 37: Polaridad de los compuestos orgánicos
Cuando el hidrógeno se une a elementos muy electronegativos, como el flúor, nitrógeno y oxígeno, los compuestos formados presentan una tendencia acusada a asociarse molecularmente ¿Esto ocurre por?
- Solubilidad de los compuestos
- Puentes de hidrógeno
- Fuerzas electrostáticas
- Dipolo momentáneo
Solución:
El efecto observado en el enunciado se explica por la formación de puentes de hidrógeno.
Un átomo de hidrógeno hace de puente entre los átomos electronegativos, sujetando a uno con un enlace covalente y al otro con fuerzas electrostáticas. Las sustancias que presentan enlaces por puentes de hidrógeno, tienen moléculas asociadas que producen un aumento en los puntos de fusión y de ebullición, con respecto a aquellas sustancias de masa molar y momentos dipolares semejantes, pero que no forman puentes de hidrógeno.
Los puentes de hidrógeno se pueden identificar en las fórmulas químicas por líneas interrumpidas.
H-F---H-F
Entre el F y el H central hay se señala la formación de un puente de hidrógeno. La línea individual (única) representa un enlace covalente.
La respuesta correcta es la opción B.
Ejercicio 38: Compuestos orgánicos, alcoholes
El etanol o alcohol etílico se obtiene correctamente por la hidratación del etileno o por fermentación del azúcar de melazas de almidón y varios granos de maíz. Es un líquido incoloro que corresponde a la fórmula molecular:
- \mathrm{C}_{3} \mathrm{H}_{6} \mathrm{OH}
- \mathrm{C}_{4} \mathrm{H}_{2} \mathrm{OH}
- \mathrm{C}_{9} \mathrm{H}_{6} \mathrm{OH}
- \mathrm{C}_{2} \mathrm{H}_{5} \mathrm{OH}
Solución:
El etanol, alcohol etílico o alcohol de granos se representa por la fórmula molecular \mathrm{C}_{2} \mathrm{H}_{5} \mathrm{OH} y su fórmula semidesarrollada es \mathrm{CH}_{3}-\mathrm{CH}_{2} \mathrm{OH} .
El alcohol etílico es el que se emplea en las bebidas alcohólicas. Su ingestión parece tener efectos estimulantes, ya que uno de los primeros síntomas en aparecer cuando se consume es la disminución de la actividad cerebral en la corteza prefrontal, donde se centraliza la inhibición y la moderación.
También se emplea como solvente en la preparación de fármacos y productos químicos; cómo antiséptico tiene mayor eficacia a una concentración de 70% v/v.
La respuesta correcta es la opción D.
Ejercicio 39: Reacciones orgánicas
¿Cuál de las siguientes reacciones orgánicas representa una reacción de eliminación?
- \mathrm{CH}_{3} \mathrm{CH}_{2} \mathrm{Br}+\mathrm{NaCN} \rightarrow \mathrm{CH}_{3} \mathrm{CH}_{2} \mathrm{CN}+\mathrm{NaBr}
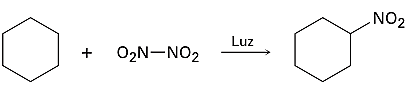
- \mathrm{CH}_{4}+\mathrm{Cl}_{2} \rightarrow \mathrm{CH}_{3} \mathrm{Cl}+\mathrm{HCL}
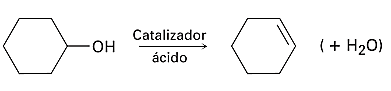
Solución:
Para identificar las reacciones de eliminación debes evaluar los reactantes y cómo se transforman cuando pasan a productos. Estas ocurren cuando un reactivo “único” se separa en dos productos y por lo general se forma agua.
La única reacción que cumple con la descripción es la que se encuentra en la opción D.

Allí podemos observar como un reactivo único se transforma en dos productos.
La respuesta correcta es la opción D.
Ejercicio 40: Polaridad de los compuestos
El enlace N–N es:
- Iónico
- Polar
- Puente de hidrógeno
- No polar
Solución:
Cuando los dos átomos que participan en un enlace son de la misma especie química, como es el caso N–N, poseen electronegatividades iguales, es decir la misma tendencia de atraer electrones, como resultado los electrones se ubican simétricamente entre los dos núcleos; formando un enlace no polar o apolar.
La respuesta correcta es la opción D.

