¿Vas a aplicar a alguna de las carreras del Área 2 en la UNAM? En este mini examen simulacro vamos a poner a prueba tus conocimientos en la materia de Química con 10 reactivos diseñados para medir qué tan listo estás para enfrentar tu examen de admisión.

¿Cómo saber si esto me sirve?
Estos reactivos han sido revisados y actualizados tomando como base la última guía oficial del examen de admisión a la UNAM.
- Reactivo 1: Mezclas homogéneas y heterogéneas
- Reactivo 2: Clasificación de elementos (metales, no metales y metaloides)
- Reactivo 3: Electronegatividad y tipos de enlace
- Reactivo 4: Reacciones ácido-base (Neutralización)
- Reactivo 5: Cálculo de masa molar (mol)
- Reactivo 6: Propiedades físicas del agua
- Reactivo 7: Indicadores y pH
- Reactivo 8: Reacciones de óxido-reducción
- Reactivo 9: Lípidos (Almacén de energía)
- Reactivo 10: Reacciones exotérmicas y endotérmicas
¡Hey, si no nos crees, échale un ojo a la última guía, ahí vas a encontrar todos estos temas!
Instrucciones
- Dispones de 2 minutos para responder cada pregunta.
- Al seleccionar la opción que consideras correcta, podrás ver inmediatamente la explicación detallada.
- Al finalizar obtendrás tu resultado total.
Puedes realizar este mini examen tantas veces como quieras. ¡Aprovéchalo para aprender y mejorar!
Reactivo 1: Mezclas
Una medalla de bronce es un ejemplo de:
Solución:
Una mezcla se forma por la unión de dos o más sustancias en diversas proporciones. La mezcla formada presenta características propias, diferentes a las de sus componentes; estas características varían según las proporciones en que se encuentren las sustancias que la forman. Si los componentes de una mezcla no se pueden diferenciar a simple vista o usando un microscopio, se dice que la mezcla es homogénea (como las aleaciones metálicas o las disoluciones). Sin embargo, si sus componentes se pueden distinguir, se habla de que la mezcla es heterogénea (como una ensalada o agua con aceite).
Al observar una medalla de bronce (una aleación, principalmente de cobre y estaño), no podemos diferenciar en ella distintas fases o componentes a simple vista, por lo que corresponde a una mezcla homogénea. Aunque comúnmente se nombran por un metal, las medallas olímpicas suelen ser aleaciones: la de bronce contiene mayoritariamente cobre, con adiciones de zinc y estaño; la de oro olímpica actual es principalmente plata (~92.5%) bañada en oro; y la de plata contiene aproximadamente 92.5% de este metal, complementado usualmente con cobre.
La respuesta correcta es la opción B.
Reactivo 2: Clasificación de los elementos: metales, no metales y metaloides
Es un elemento dúctil, maleable y presenta brillo:
Solución:
Las propiedades mencionadas (ductilidad, maleabilidad y brillo) son características típicas de los metales.
- Ne (Neón) es un gas noble (no metal).
- Si (Silicio) es un metaloide.
- Ca (Calcio) es un metal alcalinotérreo.
- Br (Bromo) es un no metal (halógeno), líquido a temperatura ambiente.
El calcio (Ca), como metal, es dúctil (puede formar hilos), maleable (puede formar láminas) y presenta brillo metálico característico (aunque se oxida rápidamente en contacto con el aire húmedo, perdiendo su lustre inicial).
La respuesta correcta es la opción C.
Reactivo 3: Electronegatividad y tipo de enlace
Al enlace que se forma entre dos átomos con igual valor de electronegatividad se le llama:
Solución:
La electronegatividad mide la tendencia de un átomo a atraer electrones en un enlace químico. La diferencia de electronegatividad (\Delta EN) entre los átomos enlazados determina el tipo de enlace:
- Enlace iónico: Se forma entre átomos con una gran diferencia de electronegatividad (\Delta EN > 1.7 aproximadamente), usualmente entre un metal y un no metal, donde hay transferencia de electrones.
- Enlace covalente: Se forma cuando los átomos comparten electrones. Se subdivide en:
- Covalente no polar: Ocurre cuando los átomos tienen electronegatividades iguales o muy similares (\Delta EN \approx 0). Los electrones se comparten de forma equitativa. Esto sucede típicamente entre átomos idénticos (ej. H_2, Cl_2, O_2).
- Covalente polar: Ocurre cuando hay una diferencia apreciable de electronegatividad (0 < \Delta EN \leq 1.7 aprox.), pero no suficiente para la transferencia completa. Los electrones se comparten de forma desigual, creando polos parciales en la molécula.
- Enlace metálico: Se da entre átomos metálicos, formando una red donde los electrones de valencia están deslocalizados (“mar de electrones”).
- Puente de hidrógeno: Es una interacción intermolecular (no un enlace intramolecular primario) fuerte entre un átomo de H unido a un átomo muy electronegativo (N, O, F) y otro átomo electronegativo cercano.
Cuando dos átomos tienen igual valor de electronegatividad (\Delta EN = 0), el enlace formado es covalente no polar, ya que los electrones son compartidos de manera perfectamente equitativa.
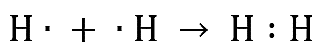
La respuesta correcta es la opción D.
Reactivo 4: Compuestos químicos
¿Qué ecuación química representa la formación de una sal mediante neutralización?
Solución:
La formación de una sal mediante una reacción de neutralización ocurre típicamente por la combinación de un ácido con una base, produciendo la sal y agua.
Analicemos las opciones:
- a) SO_2 + H_2O \to H_2SO_3 : Un óxido ácido reacciona con agua para formar un ácido (ácido sulfuroso).
- b) Cl_2 + H_2 \to 2HCl : Elementos reaccionan para formar un ácido (ácido clorhídrico).
- c) N_2O_5 + H_2O \to 2HNO_3 : Un óxido ácido reacciona con agua para formar un ácido (ácido nítrico).
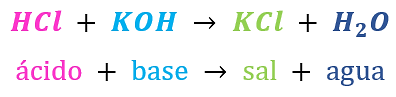
- d) HCl + KOH \to KCl + H_2O : Un ácido (HCl, ácido clorhídrico) reacciona con una base (KOH, hidróxido de potasio) para formar una sal (KCl, cloruro de potasio) y agua.
La ecuación que representa la formación de una sal por neutralización es la de la opción D.
La respuesta correcta es la opción D.
Reactivo 5: Cálculos estequiométricos
¿Cuántos moles hay en 100 g de NaCl?
Solución:
Para calcular los moles de Cloruro de Sodio (NaCl) presentes en 100 gramos del compuesto, primero necesitamos determinar su masa molar (comúnmente llamada peso molecular).
Utilizamos las masas atómicas de los elementos (aproximadas):
- Masa atómica del Sodio (Na): 23.0 g/mol
- Masa atómica del Cloro (Cl): 35.5 g/mol
La masa molar del NaCl es la suma de las masas atómicas de sus componentes:
Masa \, Molar \, (NaCl) = (1 \times 23.0 \, \frac{g}{mol}) + (1 \times 35.5 \, \frac{g}{mol}) = 58.5 \, \frac{g}{mol}
Esto significa que 1 mol de NaCl tiene una masa de 58.5 gramos.
Ahora, podemos calcular cuántos moles hay en 100 gramos utilizando la relación:
Moles = \frac{Masa \, (g)}{Masa \, Molar \, (\frac{g}{mol})}
Moles \, de \, NaCl = \frac{100 \, g}{58.5 \, \frac{g}{mol}} \approx 1.7094 \, mol
Redondeando, en 100 g de NaCl hay aproximadamente 1.71 moles del compuesto.
La respuesta correcta es la opción B.
Reactivo 6: Propiedades físicas de los líquidos
Propiedad del agua gracias a la cual un insecto puede caminar sobre ella:
Solución:
Las moléculas en el interior de un líquido son atraídas en todas direcciones por las fuerzas intermoleculares (cohesión). Sin embargo, las moléculas en la superficie experimentan una fuerza neta hacia el interior del líquido, ya que hay menos moléculas por encima de ellas para atraerlas hacia arriba. Esta fuerza neta hacia el interior hace que la superficie del líquido se comporte como una membrana elástica tensa.
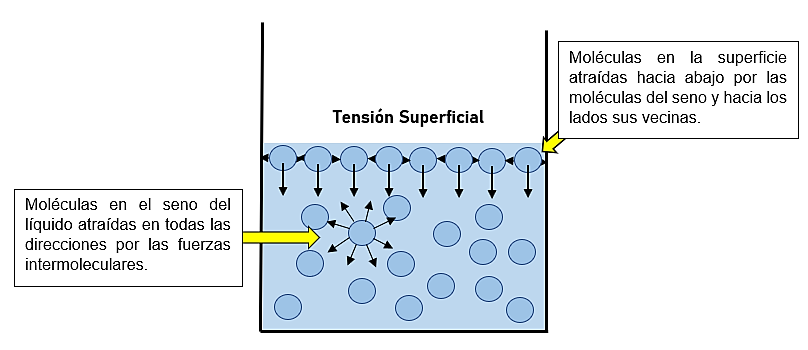
Esta propiedad, llamada tensión superficial, es la responsable de la forma esférica de las gotas pequeñas y permite que objetos ligeros, como algunos insectos (ej. zapateros), puedan “caminar” sobre la superficie del agua sin hundirse, ya que su peso no es suficiente para romper esa “membrana” superficial.
Si bien la polaridad y los puentes de hidrógeno del agua contribuyen a su alta tensión superficial, la propiedad directamente responsable del fenómeno descrito es la tensión superficial en sí misma.

La respuesta correcta es la opción B.
Reactivo 7: Acidez y alcalinidad
Al agregar unas gotas de vinagre (pH ≈ 3.5) a un litro de agua pura (pH = 7), el pH de la disolución resultante probablemente será:
Solución:
El agua pura tiene un pH neutro de 7. El vinagre es una disolución acuosa de ácido acético, y tiene un pH ácido (el enunciado indica ≈ 3.5).
Al añadir una pequeña cantidad de una sustancia ácida (vinagre) a un volumen grande de una sustancia neutra (agua), la concentración de iones hidrógeno (H^+) en la mezcla aumentará ligeramente con respecto al agua pura, y por lo tanto, el pH disminuirá.
Sin embargo, como la cantidad de ácido añadido (“unas gotas”) es muy pequeña en comparación con el volumen de agua (1 litro), el cambio en el pH no será drástico. La disolución resultante no llegará a ser tan ácida como el vinagre puro, ni permanecerá neutra. El pH final estará entre el pH del vinagre y el pH del agua, resultando en una disolución ligeramente ácida (un pH algo menor que 7, pero significativamente mayor que 3.5).
La respuesta correcta es la opción B.
Reactivo 8: Reacciones de óxido-reducción
Cuando el carbono (C) se combina con el oxígeno (O_2) para formar dióxido de carbono (CO_2), ocurre que:
Solución:
Las reacciones de óxido-reducción (Redox) involucran la transferencia de electrones entre especies químicas, lo que resulta en un cambio en sus números de oxidación.
- Oxidación: Es la pérdida de electrones, lo que conlleva un aumento en el número de oxidación. La especie que se oxida actúa como agente reductor.
- Reducción: Es la ganancia de electrones, lo que conlleva una disminución en el número de oxidación. La especie que se reduce actúa como agente oxidante.
Analicemos la reacción de formación de CO_2:
C_{(s)} + O_{2(g)} \to CO_{2(g)}
Asignamos los números de oxidación:
- En los reactivos, C y O (como elementos puros) tienen número de oxidación 0: C^0, O_2^0 .
- En el producto (CO_2), el oxígeno usualmente tiene número de oxidación -2. Para que la molécula sea neutra, el carbono debe tener +4: C^{+4}O_2^{-2} .
Observamos los cambios:
- Carbono (C): Pasa de 0 a +4. Su número de oxidación aumenta, por lo tanto, se oxida (pierde electrones).
- Oxígeno (O): Pasa de 0 a -2. Su número de oxidación disminuye, por lo tanto, se reduce (gana electrones).
Por lo tanto, el carbono se oxida al perder electrones y el oxígeno se reduce al ganar electrones.
La respuesta correcta es la opción C.
Reactivo 9: Biomoléculas
Biomoléculas que sirven principalmente como reserva energética a largo plazo en los organismos:
Solución:
Las biomoléculas cumplen diversas funciones en los organismos vivos. En cuanto a la reserva energética:
- Carbohidratos: Son la fuente principal de energía inmediata para las células (ej. glucosa). También sirven como reserva energética a corto plazo (ej. glucógeno en animales, almidón en plantas).
- Lípidos: Son la principal forma de reserva energética a largo plazo en animales (grasas) y plantas (aceites). Almacenan más energía por gramo que los carbohidratos. Además, cumplen funciones estructurales (membranas celulares), de aislamiento térmico y hormonales.
- Aminoácidos: Son los monómeros de las proteínas. Su función principal es estructural y catalítica (enzimas), aunque pueden ser utilizados como fuente de energía en situaciones excepcionales. No son una forma primaria de reserva energética.
- Vitaminas: Son compuestos orgánicos esenciales en pequeñas cantidades para diversas funciones metabólicas, pero no actúan como reserva energética.
Por lo tanto, las biomoléculas que sirven fundamentalmente de reserva energética (especialmente a largo plazo) son los lípidos.
La respuesta correcta es la opción B.
Reactivo 10: La energía y las reacciones químicas
Las reacciones de combustión son ________ porque ________ energía calorífica hacia los alrededores.
Solución:
En termoquímica, las reacciones se clasifican según el intercambio de calor con el entorno:
- Reacciones Exotérmicas: Son aquellas que liberan energía, generalmente en forma de calor, hacia los alrededores. El cambio de entalpía (\Delta H) es negativo.
- Reacciones Endotérmicas: Son aquellas que absorben energía, generalmente en forma de calor, desde los alrededores. El cambio de entalpía (\Delta H) es positivo.
Las reacciones de combustión (como quemar madera, gas natural, etc.) son procesos que típicamente involucran la reacción rápida de una sustancia con un oxidante (usualmente oxígeno) para producir calor y luz. Son ejemplos clásicos de reacciones que desprenden una cantidad significativa de energía al entorno.
Por lo tanto, las reacciones de combustión son exotérmicas porque liberan energía calorífica hacia los alrededores.
La respuesta correcta es la opción A.

