¿Sabías que existe un estado de la materia que nos aporta vitamina D? Descubre cada detalle a lo largo del post y entérate de cosas fascinantes.

La química es el estudio del cambio, conocer la materia, sus propiedades y estados es indispensable para avanzar hacia temas complejos de la disciplina.
¿Qué es la materia?
Todos los materiales que nos rodean tienen materia y ésta se encuentra en diferentes estados de agregación.
Concepto de estados de la materia
Un “estado de la materia” es una forma de describir el comportamiento de los átomos y moléculas en una sustancia. Sus características están sujetas a las condiciones de presión y temperatura.

Los 5 estados de la materia
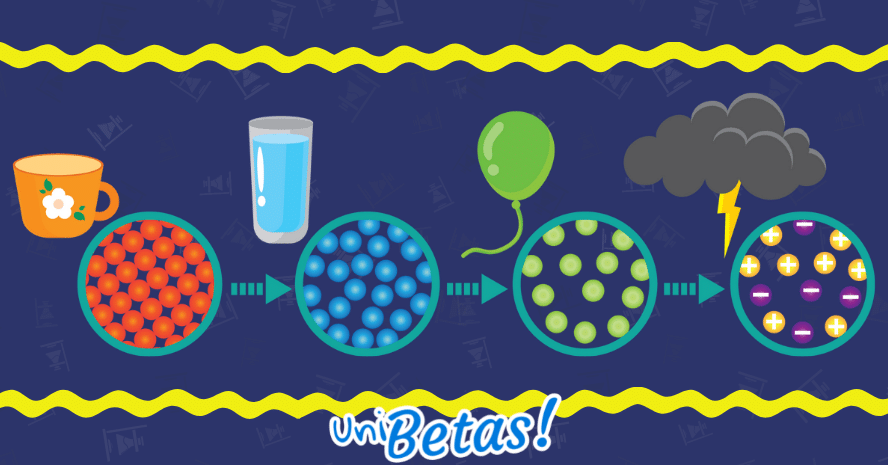
Los estados de agregación de la materia que todos conocemos son sólidos, líquidos y gaseosos. Existe un cuarto estado menos popular, el plasma y la ciencia presentó en años recientes un quinto estado llamado condensación de Bose-Einstein.
Estado sólido
Los electrones de cada átomo tienen un nivel de energía basal que les otorga una ligera vibración mientras se mantienen en un punto fijo.
Los sólidos poseen:
- Forma definida, tienen un patrón regular.
- Energía cinética muy baja.
- Masa y volumen.
- No se adaptan a la forma de los recipientes.
- Alta densidad, lo que significa que las partículas están muy cercanas entre sí.
Por ejemplo: los materiales sólidos, macizos y duros como el martillo están hechos de átomos que tienen una fuerte atracción entre ellos.
Estado líquido
Las moléculas de un líquido están cerca unas de otras, sin que se mantengan en una posición rígida, por lo que pueden moverse.
Algunas características del estado líquido son:
- Adoptan la forma de su recipiente.
- Poseen una densidad inferior a los sólidos.
- Son difíciles de comprimir.
La crema de afeitar mantiene su forma cuando no se encuentra en un recipiente, por ejemplo, si aplicamos un poco en una superficie plana y hacemos un montículo, este no perderá su forma ¿Eso quiere decir que es un sólido?
No. Si miras muy de cerca la crema de afeitar, en realidad es un líquido que contiene muchas burbujas de gas diminutas. Así que en realidad es una mezcla de un líquido y un gas que juntos mantienen su forma como un sólido… hasta que lo tocas.
Estado gaseoso
- La materia en estado gaseoso no posee una forma o volumen determinada, como en el estado sólido.
- Las partículas que conforman un gas cuando no se encuentran limitadas en un área o recipiente se separan de forma indefinida.
Por otro lado, si el gas se encuentra en un contenedor éste se expandirá en todo el interior hasta ocuparlo por completo
- Cuando se somete a presión un gas reduciendo el volumen del recipiente, se disminuye el espacio entre las partículas y se comprime el gas.
Por ejemplo, una botella de plástico con tapa sin nada en su interior, realmente no esta vacía. La botella contiene aire. El gas en su interior está formado por partículas diminutas llamadas moléculas. Si se coloca un globo en la boquilla de la botella en lugar de una tapa, y se aprieta el cuerpo de la botella, el globo se inflará por el movimiento de las moléculas de gas hacia su interior.
Plasma
Sin embargo, muchos investigadores consideran que no es un estado de la materia común en el planeta tierra. Se asocia mucho más al estado de la materia que existe en el espacio/universo.
Por ejemplo, las estrellas son en esencia bolas de plasma de elevadas temperaturas. Una estrella que vemos, sentimos y nos nutre de vitamina D a diario es el sol.
- La energía cinética del plasma es muy alta.
- Contiene partículas altamente cargadas que se mueven a gran velocidad.
Los gases nobles (helio, argón, neón, criptón, xenón y radón) se utilizan para hacer señales luminosas mediante el uso de electricidad ionizandolas hasta el estado de plasma.
Condensado de BOSE-EINSTEIN
El condensado de Bose-Einstein fue creado por los científicos Eric Cornell y Carl Weiman en el año 1995. Utilizaron una combinación de láseres e imanes para enfriar una muestra de rubidio a unos pocos grados del cero absoluto.
A una temperatura tan baja, el movimiento de las moléculas está cerca de detenerse y como no hay energía cinética transfiriéndose de un átomo a otro por la ralentización de las partículas,los átomos se agrupan progresivamente hasta formar un “súper átomo”.
Un condensado de Bose-Einstein se utiliza para:
- Estudiar la mecánica cuántica a nivel macroscópico. Se ha comprobado que la luz aparenta disminuir su velocidad cuando atraviesa el “súper átomo” lo que permite a los investigadores analizar la dualidad onda/partícula de la luz.
- Estudiar las condiciones que pudiesen existir en los agujeros negros mediante simulación.
Estados de la materia más allá de lo común
- Superfluido: Se forma cuando un líquido es enfriado casi al cero absoluto, lo que permite su fluidez sin fricción con la superficie.
- Superconductor: Es un estado de la materia que se alcanza cuando metales específicos se enfrían a temperaturas muy bajas y la electricidad se mueve a través de ellos sin resistencia.
- Materia degenerada: Un estado de la materia fuera de este planeta, sólo se forma bajo presiones inimaginablemente altas alcanzadas por estrellas muertas, como las estrellas de neutrones y las enanas blancas.
- Plasma de quark-gluones: Un estado en el que los protones y los neutrones se disuelven en sus quarks constituyentes, que pueden moverse libremente entre las partículas llamadas gluones que llevan la fuerza fuerte.
Cambios de estado de la materia
Adicionar o quitar energía de la materia provoca un cambio físico a medida que la materia pasa de un estado a otro.
Fusión
Al aplicar calor a un sólido, sus partículas comienzan a vibrar más rápido y se separan. Cuando la sustancia llega a una combinación de presión y temperatura específica, el estado sólido cambia al estado líquido (punto de fusión).
En este sentido, si dos estados de la materia, como sólido y líquido, están a la temperatura y presión de equilibrio, el calor agregado no incrementará la temperatura de la sustancia hasta que el sólido se haya transformado en líquido.
Por ejemplo, al poner hielo en un vaso de agua y dejarlo a temperatura ambiente, el hielo se irá derritiendo progresivamente hasta que el agua y el hielo tengan la misma temperatura.
A medida que el hielo se derrite por el calor proveniente del agua, permanecerá a 0° C hasta que todo el cubo de hielo se derrita antes de continuar calentándose por la influencia del agua.
Solidificación
Al eliminar el calor de un líquido, sus partículas se vuelven lentas y comienzan a asentarse en un lugar dentro de la sustancia.
Si la temperatura es lo suficientemente baja, a una presión determinada, se manifiesta el punto de congelación y el estado líquido se vuelve sólido.
Sublimación
Se presenta cuando la temperatura de una sustancia aumenta a gran velocidad, superando el punto de ebullición.
La liofilización de sustancias es un proceso que se utiliza para eliminar el agua de una mezcla, dicha muestra se enfría en condiciones de vacío para que el agua de la sustancia se sublime.
Algunas sustancias volátiles se subliman a temperatura y presión ambiente, como el dióxido de carbono congelado o el hielo seco.

Vaporización
La vaporización es el cambio de un estado líquido a un estado gaseoso y ocurre cuando se alcanza el punto de ebullición de una sustancia.
Durante el proceso de ebullición, la temperatura de la sustancia permanece constante.
Condensación
La condensación ocurre cuando un gas pierde energía y se une para formar un líquido. Por ejemplo, el vapor de agua se condensa en agua líquida, lo que se conoce como punto de rocío.
Deposición
La deposición se produce cuando un gas se transforma directamente en sólido, sin pasar por la fase líquida. El vapor de agua se convierte en hielo o escarcha cuando el aire que toca un sólido está más frío que el resto del aire.

