¡Hola aspirante! Hoy vamos a explorar el temario y ejercicios de Química que vienen en la nueva guía para el examen UNAM 2025 del área 2. Esta materia es superimportante, pues está presente en prácticamente todas las carreras de ciencias de la salud.

Temario área 2 química
En el examen tendrás que resolver 13 preguntas de química. Y ojo – el temario oficial incluye más de 50 subtemas que van desde los conceptos básicos de la materia hasta las complejas reacciones orgánicas.
- Temas básicos
- Sustancias químicas
- Sustancias puras: elemento y compuesto
- Mezclas: homogéneas y heterogéneas
- Estructura atómica
- Conceptos de átomo, protón, electrón, neutrón, número atómico y masa atómica
- Orbitales atómicos
- Configuraciones electrónicas
- Tabla periódica
- Clasificación de elementos: metales, no metales y metaloides
- Regla del octeto de Lewis
- Propiedades periódicas
- Electronegatividad y tipos de enlace: iónico y covalente
- Energía de ionización
- Afinidad electrónica
- Clasificación de los compuestos en óxidos básicos, óxidos ácidos (anhídridos), ácidos, bases y sales
- Mol
- Concepto
- Cálculo de masa molar
- Sustancias químicas
- Agua
- Composición del agua y estructura molecular
- Polaridad y puentes de hidrógeno
- Propiedades físicas: puntos de ebullición y de fusión, capacidad calorífica específica
- Propiedades químicas: tipo de enlace, capacidad (poder) disolvente del agua
- Ácidos y bases
- Teorías ácido-base: Arrhenius, Brönsted-Lowry y Lewis
- Clasificación por su conductividad: fuertes y débiles
- Diferenciación de las sustancias de acuerdo con su pH
- Indicadores y pH
- Concentración de iones [H+] y [OH- ]
- Soluciones o disoluciones
- Concepto de soluto y disolvente
- Concentración: molaridad y porcentual
- Contaminación del agua
- Principales contaminantes: físicos, químicos y biológicos
- Fuentes generadoras: industrial, urbana y agrícola
- Importancia y aplicaciones del agua para la humanidad
- Uso responsable y preservación del agua
- Composición del agua y estructura molecular
- Aire
- ¿Qué es el aire?
- Composición porcentual del aire
- Reacciones del oxígeno
- Reacciones de combustión
- Formación de óxidos básicos
- Formación de óxidos ácidos (nitrógeno, azufre y carbono)
- Reacciones de óxido—reducción
- Ciclos del oxígeno, nitrógeno y carbono
- Contaminantes del aire
- Contaminantes primarios del aire (óxidos de nitrógeno, carbono y azufre, partículas suspendidas e hidrocarburos)
- Principales fuentes generadoras (industriales, urbanas y agrícolas)
- Impacto ambiental: inversión térmica y lluvia ácida
- Alimentos
- Carbohidratos
- Estructura
- Fuente de energía de disponibilidad inmediata
- Lípidos
- Estructura
- Almacén de energía
- Proteínas
- Grupos funcionales presentes en aminoácidos
- Enlace peptídico
- Enzimas: catalizadores biológicos
- Vitaminas y minerales: fuentes e importancia
- Carbohidratos
- La energía y las reacciones químicas
- Reacciones químicas endotérmicas y exotérmicas
- Energía interna
- Entalpía
- Energía libre y espontaneidad
- Equilibrio químico: Ley de Le Chatelier
- Velocidad de reacción y factores que influyen en ella
- Química del carbono
- Carbono
- Estructura tetraédrica
- Tipos de enlace carbono-carbono: estructura y modelos
- Alcanos, alquenos, alquinos y cíclicos
- Nomenclatura
- Isomería estructural
- Grupos funcionales
- Alcohol, éter, aldehído, cetona, ácidos carboxílicos, éster, animas, amidas y compuestos halogenados
- Nomenclatura
- Reacciones orgánicas
- Reacciones de sustitución, adición y eliminación
- Reacciones de condensación e hidrólisis
- Reacciones de polimerización por adición y condensación
- Carbono
¿Te asusta la cantidad de temas? Tranquilo, vamos paso a paso. Lo fascinante de la química es que todo está conectado: desde los átomos hasta las moléculas que forman la vida misma.
Ejercicios prácticos de química
Reactivo 23
En general, en la tabla periódica los elementos con mayor carácter metálico se ubican en
- A) los periodos superiores.
- B) los periodos inferiores.
- C) las columnas de la izquierda.
- D) las columnas de la derecha.
Reactivo 24
¿Cuántos gramos equivalen a 0.5 mol de ácido fosfórico, H_3PO_4?
- A) 49
- B) 96
- C) 98
- D) 48
Reactivo 25
Sustancias que al estar en disolución donan protones.
- A) Óxidos.
- B) Ácidos.
- C) Bases.
- D) Sales.
Reactivo 26
En cierto laboratorio, se determinó que la disolución Z tiene un valor de pH = 3, por lo cual podemos decir que presenta una concentración de iones H^+ = ___ y una concentración de iones OH^- = ___.
- A) 11 y 3
- B) 3 y 11
- C) 10^{-11} y 10^{-3}
- D) 10^{-3} y 10^{-11}
Reactivo 27
Una botella de brandy de 946 mL tiene una concentración del 38% en volumen de alcohol. Los mL de alcohol presentes en la botella son
- A) 24.84
- B) 38.00
- C) 359.48
- D) 586.52
Reactivo 28
La oxidación de un elemento no metálico genera
- A) oxisales.
- B) óxidos básicos.
- C) hidróxidos.
- D) óxidos ácidos.
Reactivo 29
¿Cuál de las siguientes ecuaciones químicas representa a una reacción que favorece la formación de la lluvia ácida?
- A) C + 2H_2 \rightarrow CH_4
- B) SO_3 + H_2O \rightarrow H_2SO_4
- C) CO_2 \rightarrow C + O_2
- D) N_2 + 3H_2 \rightarrow 2NH_3
Reactivo 30
Nutrimentos que se consumen en forma de almidones y azúcares.
- A) Lípidos.
- B) Vitaminas.
- C) Carbohidratos.
- D) Proteínas.
Reactivo 31
Los triglicéridos son un grupo de lípidos caracterizados por tener el grupo funcional
- A) éter.
- B) éster.
- C) amida.
- D) alcohol.
Reactivo 32
Un valor de constante de equilibrio mayor que 1 indica que
- A) hay mayor formación de productos que de reactivos.
- B) hay mayor formación de reactivos que de productos.
- C) el equilibrio se desplaza hacia los reactivos.
- D) la reacción química está en equilibrio.
Reactivo 33
La función principal de un catalizador en una reacción química es
- A) aumentar la energía de activación.
- B) favorecer la pureza de los productos.
- C) disminuir la energía de activación.
- D) aumentar la temperatura de los reactivos.
Reactivo 34
La siguiente estructura representa a un
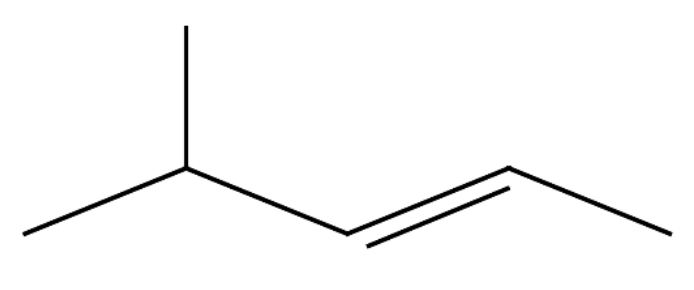
- A) alqueno.
- B) aromático.
- C) alquino.
- D) alcano.
Reactivo 35
¿Cuál de los siguientes compuestos es un ácido carboxílico?
- A)
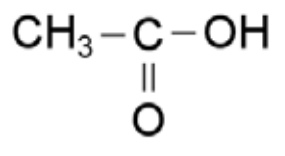
- B)
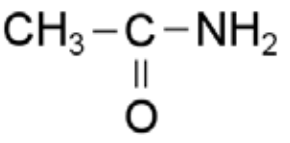
- C) CH_3-CH_2-CH_3
- D)
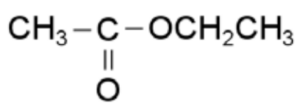
Respuestas
- Reactivo 23: C
- Reactivo 24: A
- Reactivo 25: B
- Reactivo 26: D
- Reactivo 27: C
- Reactivo 28: D
- Reactivo 29: B
- Reactivo 30: C
- Reactivo 31: B
- Reactivo 32: A
- Reactivo 33: C
- Reactivo 34: A
- Reactivo 35: A
Estrategia de estudio: ¿Por dónde comenzar?
La química puede parecer muchísima al principio, pero hay una manera práctica de abordarla. Estos son los temas que suelen ser más retadores para los aspirantes:
- – Química orgánica: Los grupos funcionales y sus reacciones pueden volverte loco si no tienes un buen método para organizarlos.
- – Equilibrio químico: El pH y las reacciones ácido-base requieren mucha práctica.
- – Estequiometría: Los cálculos moleculares suelen ser complicados, pero son la base de todo.
La ruta más efectiva para empezar:
- – Domina la tabla periódica: es tu mejor amiga en química
- – Aprende bien el concepto de mol: es la base de todos los cálculos
- – Practica el balanceo de ecuaciones: te servirá para todo
- – Familiarízate con las propiedades periódicas: te ahorrarán mucha memorización
Un consejo que funciona: la química está en tu vida diaria. Cuando cocinas, cuando tomas un medicamento, incluso cuando respiras, estás haciendo química. Usar estos ejemplos hace que todo sea más fácil de entender.
Y recuerda: en un examen tan competido como el de la UNAM, esas 13 preguntas de Química pueden hacer la diferencia. ¡Dale con todo y aprovecha cada momento de estudio!

