Da el primer paso para ingresar al Instituto Politécnico Nacional resolviendo los 25 reactivos de química de la guía de estudio del IPN 2023 para ciencias sociales y administrativas (CSyA).

La guía ha sido dividida en dos partes para que puedas asimilar mejor el conocimiento práctico de la materia.
A lo largo del post no solo encuentras la solución guiada de los reactivos, sino que te enseñamos la nueva estructura del examen.
Estructura del Examen IPN
Lo primero que debes conocer es que la estructura del examen al IPN 2023 ha cambiado respecto a los años anteriores. Ahora, el número de reactivos por asignatura varía según el área de conocimientos. Las áreas de estudio del Instituto Politécnico Nacional son:
- Ingeniería y Ciencias Físico Matemáticas IyCFM
- Ciencias Sociales y Administrativas CSA
- Ciencias Médico Biológias CMB
Por ello, es importante que conozcas a qué rama pertenece la carrera a la que aspiras ingresar del IPN y orientes tu ruta de aprendizaje en esa dirección.
¿Cuáles son los cambios del nuevo examen al IPN?
El examen del IPN cambio su estructura y aquí te presentamos toda la información:
- El examen evaluará la materia de inglés, específicamente en el tema de reading comprehension.
- Las materias de competencia escrita y competencia lectora, sustituyeron a producción escrita y comprensión de textos.
- Cada área asigna la cantidad de reactivos por materia.
- Se agregó la materia de historia de México a las tres áreas de estudio.
- El examen para todas las carreras tendrá 140 reactivos (anteriormente eran 130).
Estructura completa del examen:
| Materia | IyCFM | CMB | CSyA |
|---|---|---|---|
| Matemáticas | 37 | 33 | 35 |
| Competencia escrita | 20 | 20 | 25 |
| Competencia lectora | 20 | 20 | 20 |
| Reading comprehension | 10 | 10 | 10 |
| Historia | 10 | 10 | 20 |
| Biología | 9 | 17 | 10 |
| Química | 17 | 17 | 10 |
| Física | 17 | 13 | 10 |
Guía IPN: Ciencias experimentales
El área de ciencias experimentales comprende conocimientos específicos relacionados con las áreas de ciencias, entre los cuales están:
- Biología
- Química
- Física
El temario a estudiar varía entre CMB, IyCFM y CSyA. Por ello, no desperdicies el tiempo abarcando más contenido del necesario que te dejaremos a continuación.
Temario de Química
La rama de Ciencias sociales y administrativas (CSyA) tiene 4 temas menos que las que comprende CMB e IyCFM como lo ves en la siguiente tabla resumen.
| Tema | Ramas |
|---|---|
| Materia y energía | IyCFM, CMB, CSyA |
| Estructura atómica | IyCFM, CMB, CSyA |
| Elementos de la tabla periódica | IyCFM, CMB, CSyA |
| Enlace químico | IyCFM, CMB, CSyA |
| Nomenclatura química inorgánica | IyCFM, CMB, CSyA |
| Reacciones químicas inorgánicas | IyCFM, CMB, CSyA |
| Reacciones químicas | IyCFM, CMB, CSyA |
| Estequiometría | IyCFM, CMB, CSyA |
| Estructura y nomenclatura de compuestos orgánicos | IyCFM, CMB, CSyA |
| Reacciones químicas de compuestos orgánicos | IyCFM, CMB, CSyA |
| Estado gaseoso | IyCFM, CMB, CSyA |
| Disoluciones | IyCFM, CMB |
| Electroquímica | IyCFM, CMB |
| Termodinámica | IyCFM, CMB |
| Velocidad de reacción y equilibrio químico | IyCFM, CMB |
| Ácidos bases | IyCFM, CMB, CSyA |
¿Es difícil ser admitido en el IPN?
La respuesta es “depende de ti”. La práctica hace al maestro, mientras más familiarizado estés con los temas de conocimientos generales y específicos que vienen en el examen, mayor será tu seguridad.
Otro punto a considerar es que mientras mayor demanda tenga la carrera a la que aspiras, el nivel de competencia es superior.
Sin embargo, resulta complicado ser admitido en el IPN porque es una de las instituciones más demandadas del país y a pesar de tener dos vueltas, cuenta con una sola convocatoria cada año y solo tienes 3 horas para responder los 140 reactivos de la prueba.
¿Cómo resolver la guía del IPN 2023?
Antes de iniciar con la solución de los reactivos, te recomiendo examinar la bibliografía recomendada por la guía de estudio del IPN 2023. Analiza muy bien el temario para subdividir los objetivos de aprendizaje.
Para aprender de forma efectiva necesitas adoptar una metodología óptima de estudio, en donde evalúas tu grado de dominio de los puntos que vienen en el temario.
Recomendaciones para resolver la guía de estudio IPN 2023
Los siguientes tips te ayudarán a mejorar tu desempeño, en especial para contestar correctamente las preguntas de química.
- ¡Planifícate! El primer paso para iniciar el compromiso con el estudio.
- No mires la respuesta correcta. En química, encontrar la solución a algunos ejercicios prácticos puede ser difícil, pero aun así, realiza tu procedimiento antes de ver la opción correcta.
- ¡Aprender cuesta! No te frustres cuando algo no te sale a la primera, recuerda que debes establecer las conexiones neuronales para poder recordar cualquier cosa con facilidad, y eso toma tiempo.
- ¡Cronométrate! Establece un tiempo no mayor a 15 minutos por cada 10 reactivos.
- La química se trata de ensayo y error. Por ello, la forma más efectiva de aprender es resolviendo muchos ejercicios de cada tema particular.
- La ley de conservación de la masa y las propiedades de la materia son temas esenciales en el desarrollo de reactivos de química, por ello, estúdialos a fondo.
Reactivo 1
Relacionar el número cuántico con su significado.

- 1D, 2C, 3B, 4A
- 1D, 2C, 3A, 4B
- 1A, 2B, 3C, 4D
- 1A, 2B, 3D, 4C
Solución:
Cada conjunto de números cuánticos define una función específica para un electrón. En ese sentido, las relaciones son las siguientes:
- Número cuántico “l” define la energía de los subniveles en que se divide cada nivel. Relación 1D.
- Número cuántico “s” indica el sentido del giro del electrón. Relación 2C.
- Número cuántico “n” define la energía del nivel principal donde podría estar el electrón.
- Número cuántico “m” representa la posible orientación de los subniveles en el campo magnético.
Con base en las relaciones 1D, 2C, 3A, 4B la respuesta correcta es la opción B.
Reactivo 2
El empañado de las gafas de buceo y el vapor de la respiración, son ejemplos de:
- Fusión.
- Sublimación.
- Solidificación.
- Condensación.
Solución:
Cuando desciende la temperatura de un gas la energía cinética promedio de sus moléculas disminuye, en consecuencia, mientras más baja la temperatura, las moléculas ya no tienen la energía suficiente para liberarse de la fuerza de atracción hacia las moléculas vecinas. En ese momento, se forman pequeñas gotitas de líquido por el cambión de gas a líquido. Dicho fenómeno se conoce como condensación y se observa en las gafas de buceo empañadas y el vapor de la respiración.
Respuesta correcta opción D.
Reactivo 3
El estado de agregación __________ presenta forma y volumen definidos, con elevadas fuerzas de cohesión, elementos que dan lugar a una estructura interna cristalina.
- Líquido.
- Gaseoso.
- Volátil.
- Sólido.
Solución:
El estado de agregación sólido presenta forma y volumen definidos, con elevadas fuerzas de cohesión, elementos que dan lugar a una estructura interna cristalina. Tiene una alta rigidez porque sus partículas están muy cercas unas de otras.
Respuesta correcta opción D.
Reactivo 4
La destilación se utiliza para separar líquidos __________ con diferentes puntos de ebullición y, debido a la variación en la temperatura se ____________ los vapores que se desprenden durante el proceso.
- Inmiscibles – condensan
- Inmiscibles – precipitan
- Miscibles – condensan
- Inmiscibles – precipitan
Solución:
La destilación es una técnica para separar dos líquidos miscibles entre sí con diferentes puntos de ebullición. Amerita la aplicación de procesos físicos como la evaporación y la condensación.
Con la destilación se realiza la separación de dos líquidos presentes en una mezcla homogénea. Mientras mayor es la diferencia entre los puntos de ebullición de cada sustancia, mejor será la separación de los líquidos destilados.
En este sentido, el enunciado se responde de la siguiente manera:
La destilación se utiliza para separar líquidos miscibles con diferentes puntos de ebullición y, debido a la variación en la temperatura se condensan los vapores que se desprenden durante el proceso.
Respuesta correcta opción C.
Reactivo 5
Identificar la ecuación que cumple con la Ley de la conservación de la masa:
- {H}_{2}+{O}_{2} \to {H}_{2}O
- {H}_{2}+{O}_{2} \to 2{H}_{2}O
- 2{H}_{2}+{O}_{2} \to 2{H}_{2}O
- 2{H}_{2}+2{O}_{2} \to 2{H}_{2}O
Solución:
La ley de la conservación de la masa se evidencia a través de una ecuación química correctamente balanceada, en ese sentido, evaluamos las reacciones de las opciones:
{H}_{2}+{O}_{2} \to {H}_{2}O
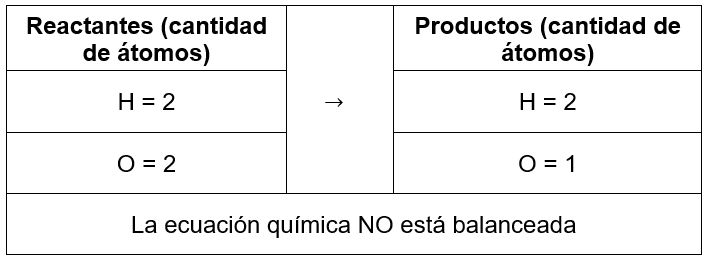
{H}_{2}+{O}_{2} \to 2{H}_{2}O
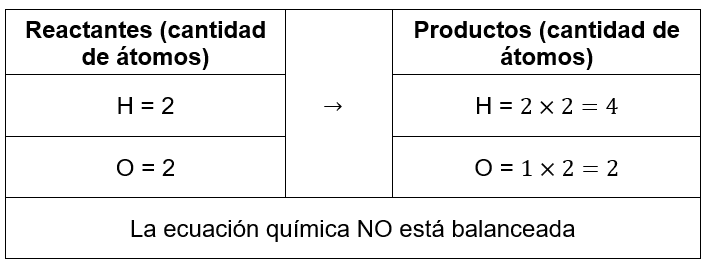
2{H}_{2}+{O}_{2} \to 2{H}_{2}O
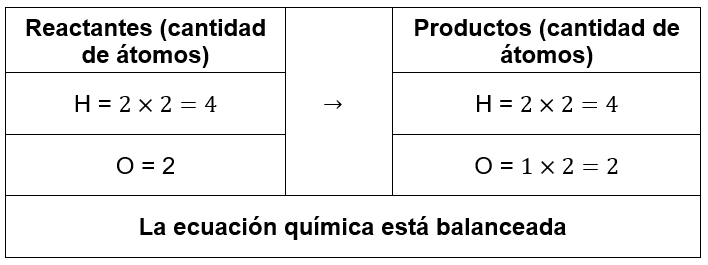
2{H}_{2}+2{O}_{2} \to 2{H}_{2}O
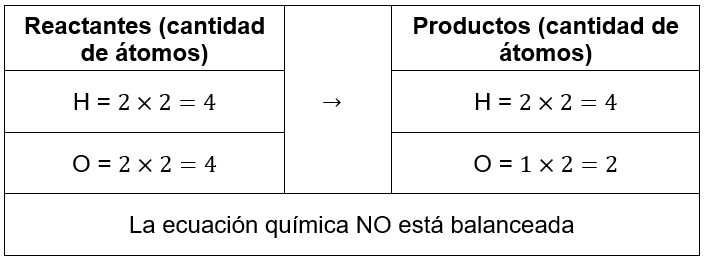
La respuesta correcta es la opción C.
Reactivo 6
Determinar los coeficientes estequiométricos de la ecuación:
___ Al+ ___ {O}_{2}\to ___ A{l}_{2}{O}_{3}
- 2, 4, 6
- 2, 1, 1
- 4, 3, 1
- 4, 3, 2
Solución:
Para conocer los coeficientes estequiométricos determinamos la cantidad de átomos a ambos lados de la reacción:
___ Al+ ___ {O}_{2}\to ___ A{l}_{2}{O}_{3}
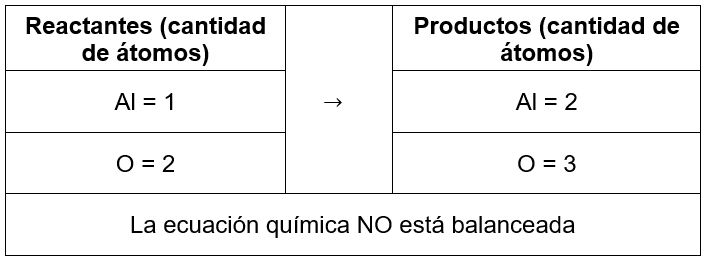
Para balancear la ecuación por tanteo, simplemente vamos a ir probando valores numéricos sencillos que al ser multiplicados por la cantidad de átomos igualen la cantidad de los mismos en los reactantes y productos:
___ Al+ ___ {O}_{2}\to ___ A{l}_{2}{O}_{3}
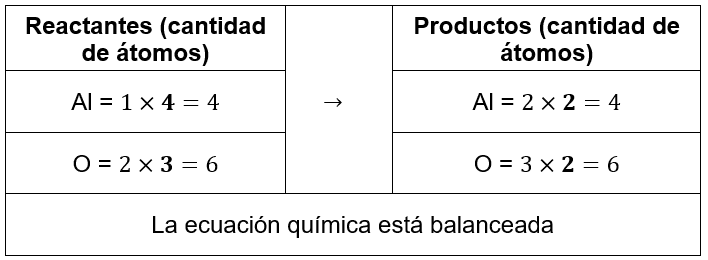
Por lo tanto, los coeficientes correspondientes son:
4A{l}_{2}+3{O}_{2}\to 2A{l}_{2}{O}_{3}
Respuesta correcta opción D.
Reactivo 7
Identificar los compuestos que presentan enlace covalente en la siguiente imagen:
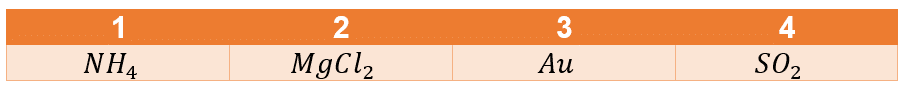
- 1, 2
- 1, 4
- 3, 4
- 3, 1
Solución:
El enlace covalente es la unión entre dos o más átomos que comparten uno o más pares de electrones. Se forma entre elementos que tienen electronegatividades cercanas, de modo que ninguno atrae a los electrones con suficiente fuerza como para mantenerlo en órbita sobre su propio núcleo.
En este caso los electrones que participan del enlace se mantienen girando alrededor de los núcleos de los átomos que comparten. Ejemplos de ellos son:
- Los óxidos no metálicos como el S{O}_{2}
- Compuestos moleculares como el amonio N{H}_{4}
Repuesta correcta opción B.
Reactivo 8
Seleccionar el tipo de enlace que presenta la molecula de agua.
- Iónico.
- Metálico.
- Covalente polar.
- Covalente no polar.
Solución:
El enlace covalente polar sucede cuando el comportamiento de los electrones se ve afectado por una diferencia de electronegatividades entre los elementos de la molécula.
En un compuesto covalente que cuenta con un átomo más electronegativo, como la presencia del oxígeno en la molécula de agua, los electrones se acercarán al él generando una zona de densidad negativa δ- y una zona de densidad positiva δ+ (sobre los elementos de menor electronegatividad, es decir, los hidrógenos).
En otras palabras, el enlace covalente polar se basa en el principio de que los electrones pasan más tiempo alrededor de un átomo que de otro.
Respuesta correcta opción C.
Reactivo 9
Relacionar el compuesto con su uso industrial.

- 1A, 2B, 3C
- 1B, 2A, 3C
- 1B, 2C, 3A
- 1A, 2C 3B
Solución:
La industria química utiliza compuestos orgánicos e inorgánicos para fabricar todo tipo de materiales que pueden ser de uso común o especializado. Ejemplo de ellos son:
- El dióxido de azufre \left(S{O}_{2}\right) es uno de los más relevantes en la industria química utilizado en la fabricación de explosivos y sulfonación de compuestos orgánicos.
- Hidróxido de calcio \left[Ca{\left(OH\right)}_{2}\right] tiene acción bactericida y antifúngica, se utiliza en la fabricación de colas y gelatinas, conservación de frutas y verduras.
- Hidróxido de sodio (NaOH) potente alcaloide que permite la saponificación de los ácidos grasos para fabricar jabones, además se utiliza para producir papel, algodón y prendas textiles.
Respuesta correcta opción C.
Reactivo 10
La ___________ química describe los cambios de la materia debidos al reordenamiento de los átomos y la __________ química es la representación escrita y simbólica de los reactivos y productos.
- Ecuación – reacción
- Reacción – ecuación
- Reacción – formulación
- Experimentación – formulación
Solución:
La reacción química describe los cambios de la materia debidos al reordenamiento de los átomos y la ecuación química es la representación escrita y simbólica de los reactivos y productos.
Respuesta correcta opción B.

